ФІКСАПРОСТ

ІНСТРУКЦІЯ
для медичного застосування лікарського засобу
Фіксапрост
( Fixaprost®)
Склад:
діючі речовини : латанопрост, тимолол;
1 мл розчину містить 50 мкг латанопросту і тимололу малеату, що відповідає 5 мг тимололу;
допоміжні речовини: олія рицинова поліетоксильована, гідрогенізована; сорбіт (Е 420), карбомер, макрогол 4000, динатрію едетат, натрію гідроксид, вода для ін’єкцій.
Лікарська формаКраплі очні, розчин.
Основні фізико-хімічні властивості:жовтуватий опалесцентний розчин, практично вільний від часток.
Фармакотерапевтична група
Засоби, що застосовуються в офтальмології. Блокатори бета-адренорецепторів. Тимолол, комбінації. Код АТС S01E D51.Фармакологічні властивості
Механізм дії
Фіксапрост має у своєму складі два компоненти: латанопрост та тимололу малеат. Кожен з цих двох компонентів має свій механізм зниження підвищеного внутрішньоочного тиску (ВОТ), а їх комбіноване застосування спричиняє ефект додаткового зниження ВОТ порівняно з дією кожної речовини окремо.
Латанопрост, аналог простагландину F2α, є селективним агоністом простаноїдного рецептора FP, що знижує ВОТ шляхом збільшення відтоку водянистої вологи. Основним механізмом дії є посилений увеосклеральний відтік. Крім того, повідомлялось про деяке збільшення об’єму відтоку (зменшення опору трабекулярного відтоку) у людини. Латанопрост не чинить істотного впливу на продукування водянистої вологи, гематоофтальмічний бар’єр або внутрішньоочний кровообіг. Тривале лікування латанопростом очей у мавп, які пройшли екстракапсулярну екстракцію кришталика, не впливало на кровоносні судини сітківки, що доведено за допомогою флюоресцеїнової ангіографії. Латанопрост не спричиняв витікання флуоресцеїну в задньому сегменті ока людини при псевдофакії під час короткотривалого лікування.
Тимолол є бета-1 та бета-2 (неселективний) блокатором адренергічних рецепторів, що не чинить суттєвої внутрішньої симпатоміметичної дії, дії як прямого депресанта міокарда або як стабілізатора мембран. Тимолол знижує ВОТ, зменшуючи утворення водянистої вологи в циліарному епітелії.
Точний механізм дії чітко не встановлений, але є ймовірним пригнічення посиленого циклічного аденозинмонофосфату (АМФ), спричиненого ендогенною бета-адренергічною стимуляцією. Не встановлено, чи тимолол суттєво впливає на проникність гематоофтальмічного бар’єра для білків плазми. У дослідженнях з кролями тимолол не чинив впливу на регіонарний очний кровотік після тривалого лікування.
Фармакодинамічна дія
Клінічна дія
У дослідженнях з визначення дози референтний комбінований продукт латанопрост / тимолол із вмістом консерванту спричиняв суттєво більші зниження середнього добового ВОТ порівняно з латанопростом та тимололом, що застосовувались раз на добу як монотерапія. У двох добре контрольованих, подвійно сліпих шестимісячних клінічних дослідженнях ефект зниження ВОТ референтного комбінованого продукту латанопрост/тимолол із вмістом консерванту порівнювали з монотерапією латанопростом та тимололом у пацієнтів із значенням ВОТ 25 мм рт. ст. або більше. Після 2-4 тижнів попереднього застосування тимололу (середнє зниження ВОТ становило 5 мм рт. ст. від показника, зафіксованого на момент включення у дослідження), після 6 місяців лікування відповідно референтним комбінованим продуктом латанопрост / тимолол із вмістом консерванту, латанопростом та тимололом (двічі на день) у пацієнтів спостерігалося додаткове зниження середнього добового ВОТ на 3,1, 2,0 та 0,6 мм рт. ст. відповідно. Ефект зниження ВОТ референтним комбінованим продуктом латанопрост / тимолол із вмістом консерванту утримувався протягом наступних 6-місячних відкритих розширених досліджень.
Наявні дані свідчать про те, що застосування препарату увечері може бути більш ефективним для зниження ВОТ, ніж застосування препарату зранку. Однак, розглядаючи рекомендації щодо дозування вранці або ввечері, слід враховувати спосіб життя пацієнта та його ймовірну згоду.
Слід пам’ятати, що у разі недостатньої ефективності комбінованого препарату може бути ефективним призначення окремо тимололу 2 рази на добу та латанопросту 1 раз на добу, що було підтверджено під час досліджень.
Дія референтного комбінованого продукту латанопрост / тимолол із вмістом консерванту починається протягом 1 години, а максимальний ефект досягається протягом 6-8 годин. Адекватний ефект зниження ВОТ триває до 24 годин після введення дози у випадку тривалого лікування.
Клінічна ефективність і безпека
Дію лікарського засобу Фіксапрост без консерванту досліджували у 3-місячному рандомізованому сліпому дослідженні у порівнянні із дією референтного продукту латанопрост/тимолол 50 мкг / 5 мг на 1 мл із вмістом консерванту у 242 пацієнтів з очною гіпертензією або відкритокутовою глаукомою, які мали підтвердження недостатнього контролю при застосуванні монотерапії. Перед початком дослідження пацієнтів лікували та контролювали, застосовуючи референтний препарат або генеричні препарати (фіксована комбінація крапель очних латанопрост / тимолол 50 мкг / 5 мг на мл із вмістом консерванту) протягом принаймні 2 місяців.
Первинною величиною ефективності була зміна від базової лінії середнього внутрішньоочного тиску (ВОТ) на 84-й день.
На 84-й день середня зміна ВОТ від базової лінії становила -0,49 мм рт. ст. при застосуванні лікарського засобу Фіксапрост і була подібною до такої при застосуванні референтного продукту латанопрост / тимолол 50 мкг / 5 мг на мл із вмістом консерванту.
Найсильніше уражене око (mITT населення) | Фіксапрост | Референтний препарат | |
Базова лінія (день 0) | N Середнє значення ± СВ | 124 15,6 ± 2,1 | 112 15,7 ± 2,1 |
День 84 | n Середнє значення ± СВ | 122 15,1 ± 2,4 | 110 15,2 ± 2,2 |
Середня зміна (день 0 - день 84) | n Середнє значення ± СВ [95% ДІ] | 122 -0,49 ± 1,80 [-0,81 ; -0,17] | 110 -0,49 ± 2,25 [-0,92 ; -0,07] |
Статистичний аналіз | Скоректована середня різниця ± СП [95% ДІ] | 0,01 ± 0,25 [-0,48; 0,50] | |
ДI = довірчий інтервал; mITT = модифікований намір щодо лікування; N = кількість пацієнтів у групі лікування; n = кількість пацієнтів із даними; СП = стандартна похибка; СВ = стандартне відхилення
У цьому 3-місячному дослідженні не було виявлено жодних очних побічних ефектів лікарського засобу Фіксапрост, крім тих, що вже належним чином задокументовані для референтного препарату латанопрост/тимолол. Застосування Фіксапросту було пов’язано з меншою кількістю суб’єктивних симптомів при закапуванні на 84-й день (подразнення / печіння / поколювання: 20,5 % проти 41,8 %, р <0,001; свербіж: 4,9 % проти 13,9 %, р = 0,010), а також із суб’єктивними симптомами протягом дня незалежно від закапування (подразнення / печіння / поколювання: 7,4 % проти 12,7 %, р = 0,094; свербіж: 1,6 % проти 13,6 %, р <0,001) порівняно з референтним препаратом.
Кілька системних побічних реакцій, що вже були добре відомі для тимололу, але не спостерігались у клінічних випробуваннях із комбінованим референтним препаратом латанопрост / тимолол, що містить консервант (див. розділ «Побічні реакції»), спостерігалися з частотою «нечасто»: дисгевзія, аритмія та втома.
Латонапрост.
Абсорбція.
Латанопрост. Це — це ізопропіловий ефір активної речовини, тобто він є проліками, і сам по собі неактивний, але після гідролізу естеразами в рогівці до кислоти латанопросту стає біологічно активним. Він добре всмоктуються через рогівку, і весь лікарський засіб, що потрапляє у водянисту вологу, гідролізується під час проходження через рогівку.
Розподіл.Дослідження із участю людей свідчать, що максимальна концентрація у водянистій волозі, а це близько 15-30 нг/мл, досягається приблизно через 2 години після місцевого введення латанопросту. Після місцевого застосування у мавп латанопрост розподіляється переважно в передньому сегменті, кон’юнктиві та повіках.
Кліренс кислоти латанопросту у плазмі крові становить 0,4 л/год/кг; об’єм розподілу невеликий, близько 0,16 л/кг, що зумовлює короткий період напіввиведення із плазми — 17 хвилин. Після місцевого уведення в очі системна біодоступність кислоти латанопросту становить 4 5%. Кислота латанопросту зв’язується з білками плазми на 87 %.
Біотрансформація та виділення.Метаболізм кислоти латанопросту в оці практично не відбувається. Основний метаболізм відбувається в печінці. Основні метаболіти 1,2-динор і 1,2,3,4-тетранор, що практично не виявляли біологічної активності у дослідженнях на тваринах, виводяться головним чином із сечею.
Тимолол.
Абсорбція і розподіл.Максимальна концентрація тимололу у водянистій волозі ока досягається приблизно через 1 годину після місцевого застосування очних крапель. Частина дози всмоктується у системний кровотік, максимальна концентрація 1 нг/мл в плазмі крові досягається через 10-20 хвилин після місцевого введення 1 краплі в кожне око 1 раз на добу (300 мкг/доб).
Біотрансформація.Період напіввиведення тимололу в плазмі становить близько 6 годин. Тимолол інтенсивно метаболізується в печінці.
Виділення.Метаболіти разом із деякою кількістю незміненого тимололу виводяться із сечею.
Фармакокінетична/фармакодинамічна взаємодія.Фармакокінетичних взаємодій між латанопростом і тимололом не спостерігалось, хоча мало місце підвищення приблизно в 2 рази концентрації кислоти латанопросту у водянистій волозі ока через 1-4 години після застосування комбінованого продукту латанопрост / тимолол порівняно з монотерапією.
Клінічні характеристики
Показання.
Фіксапрост призначений для зниження внутрішньоочного тиску (ВОТ) у дорослих пацієнтів (в тому числі літніх людей) з відкритокутовою глаукомою та очною гіпертензією, які недостатньо чутливі до препаратів групи бета-адреноблокаторів або аналогів простагландину місцевої дії.
Протипоказання.
Фіксапрост протипоказаний пацієнтам із:
· синдромом підвищеної реактивності дихальних шляхів, у тому числі з бронхіальною астмою або бронхіальною астмою у анамнезі, тяжкими хронічними обструктивними захворюваннями легень;
· синусовою брадикардією, синдромом слабкості синусового вузла, синоатріальною блокадою, атріовентрикулярною блокадою II або III ступенів, що не піддається контролю водієм ритму, вираженою серцевою недостатністю, кардіогенним шоком;
· гіперчутливістю до активних чи будь-якої із допоміжних речовин лікарського засобу.
Взаємодія з іншими лікарськими засобами та інші види взаємодій
Специфічних випробувань щодо взаємодії Фіксапросту з іншими лікарськими засобами не проводилось.
Повідомлялося про парадоксальне підвищення внутрішньоочного тиску після одночасного місцевого застосування в очі двох аналогів простагландину. Тому не рекомендується одночасне застосування двох і більше простагландинів або аналогів простагландинів, або похідних простагландинів.
Існує ризик прояву адитивного ефекту, що може спричинити артеріальну гіпотензію та/або виражену брадикардію у випадку одночасного застосування офтальмологічних розчинів бета-блокаторів із препаратами для перорального застосування: блокаторами кальцієвих каналів, бета-адреноблокаторами, антиаритмічними препаратами (включаючи аміодарон), глікозидами наперстянки, парасимпатоміметиками і гуанетидином.
Повідомлялося про потенціювання системної бета-блокади (наприклад, зниження частоти серцевих скорочень, депресія) при комбінованому лікуванні тимололом та інгібіторами CYP2D6 (наприклад, хінідин, флуоксетин, пароксетин).
Вплив на внутрішньоочний тиск або відомі ефекти системної бета-блокади можуть посилитися, якщо Фіксапрост застосовують пацієнтам, які вже отримують пероральний бета-адреноблокатор, тому використання двох або більше бета-адреноблокаторів місцевої дії не рекомендується.
Є поодинокі повідомлення про мідріаз, що виникає в результаті одночасного застосування офтальмологічних бета-адреноблокаторів і адреналіну (епінефрину).
При прийомі бета-блокаторів може посилитися гіпертонічна реакція на раптову відміну клонідину.
Бета-адреноблокатори можуть посилювати гіпоглікемічний ефект протидіабетичних засобів, а також можуть маскувати ознаки та симптоми гіпоглікемії (див. розділ «Особливості застосування»).
Особливості застосування.
Системний вплив.
Як і інші офтальмологічні препарати місцевої дії, Фіксапрост може всмоктуватись у системний кровотік. Оскільки тимолол є бета-блокатором, можливий розвиток побічних реакцій з боку серцево-судинної, дихальної та інших систем, що можуть виникати при системному застосуванні таких препаратів. Частота проявів системних побічних реакцій після місцевого застосування офтальмологічних препаратів нижча, ніж при системному застосуванні. Щодо методів зниження системної абсорбції див. розділ «Спосіб застосування та дози».
Порушення з боку серця.
У випадку застосування бета-блокаторів пацієнтам із серцево-судинними захворюваннями (наприклад, ішемічна хвороба серця, вазоспастична стенокардія / стенокардія Принцметала, серцева недостатність) та артеріальною гіпотензією слід серйозно оцінити їх стан і розглянути можливість лікування препаратами з іншим механізмом дії. Необхідно спостерігати за станом пацієнтів із серцево-судинними захворюваннями щодо появи ознак погіршення цих захворювань і проявів побічних реакцій.
Бета-блокатори слід з обережністю призначати пацієнтам із блокадою серця I ступеня через негативний вплив на швидкість проведення імпульсу.
Повідомлялося про серцеві реакції та рідко про смерть у зв’язку з серцевими порушеннями після прийому тимололу.
Порушення з боку судинної системи.
Пацієнтам із тяжкими периферичними розладами / порушенням кровообігу (наприклад, тяжкі форми хвороби/синдрому Рейно) препарат слід застосовувати з обережністю.
Порушення з боку дихальної системи.
При застосуванні офтальмологічних бета-блокаторів у пацієнтів з астмою було зареєстровано прояви (включаючи летальні випадки від бронхоспазму) реакцій з боку дихальної системи. Фіксапрост слід з обережністю застосовувати пацієнтам із легкими/помірними хронічними обструктивними захворюваннями легень і тільки за умови, що очікувана користь перевищує потенційний ризик.
Гіпоглікемія/діабет.
Бета-блокатори слід з обережністю застосовувати пацієнтам, схильним до спонтанної гіпоглікемії, або пацієнтам із неконтрольованим діабетом, оскільки бета-блокатори можуть маскувати симптоми гострої гіпоглікемії.
Гіпертиреоз.
Бета-блокатори можуть маскувати симптоми гіпертиреозу.
Ураження рогівки.
Офтальмологічні бета-блокатори можуть спричиняти сухість очей. Пацієнтам із захворюваннями рогівки препарат слід застосовувати з обережністю.
Інші бета-блокатори.
Вплив на ВОТ або інші відомі прояви дії системних бета-блокаторів можуть посилюватися при застосуванні тимололу пацієнтами, які вже отримують системний бета-блокатор. Слід ретельно спостерігати за клінічною ефективністю при лікуванні таких пацієнтів. Застосування двох і більше бета-адреноблокаторів місцевої дії не рекомендовано (див. розділ Взаємодія з іншими лікарськими засобами та інші види взаємодій.)
Супутня терапія.
Тимолол може взаємодіяти з іншими препаратами (див. розділ «Взаємодія з іншими лікарськими засобами та інші види взаємодій»).
Інші аналоги простагландинів.
Супутнє застосування двох і більше простагландинів, аналогів простагландинів або похідних простагландинів не рекомендується (див. розділ «Взаємодія з іншими лікарськими засобами та інші види взаємодій»).
Анафілактичні реакції.
При застосуванні бета-блокаторів пацієнти, які мають атопію або тяжкі анафілактичні реакції в анамнезі на різні алергени, можуть виявляти більшу чутливість при повторному впливі таких алергенів і у разі виникнення анафілактичних реакцій можуть не реагувати на звичайні дози адреналіну, що застосовують для лікування таких реакцій.
Відшарування судинної оболонки ока.
Повідомлялося про відшарування судинної оболонки ока після проведення фільтраційних оперативних втручань і призначення лікування супресорами утворення водянистої вологи (наприклад, тимолол, ацетазоламід).
Анестезія при хірургічному втручанні.
Офтальмологічні бета-блокатори можуть блокувати системний вплив бета-агоністів, наприклад адреналіну. Анестезіолога необхідно повідомити про те, що пацієнт застосовує тимолол.
Зміни забарвлення райдужної оболонки ока.
Латанопрост може спричинити поступову зміну кольору очей за рахунок збільшення кількості коричневого пігменту у райдужній оболонці ока. Аналогічно досвіду застосування крапель очних латанопросту, посилення забарвлення райдужної оболонки ока спостерігалось у 16-20 % із усіх пацієнтів, що лікувались комбінованим референтним препаратом латанопрост / тимолол із вмістом консерванту на протязі до одного року (дані на основі фотографій).
Цей ефект спостерігається переважно у хворих зі змішаним забарвленням райдужної оболонки, наприклад зелено-коричневим, жовто-коричневим або блакитно/сіро-коричневим, і зумовлений підвищеним вмістом меланіну у стромальних меланоцитах райдужної оболонки. Як правило, коричнева пігментація навколо зіниці поширюється концентрично у напрямку периферії ураженого ока, проте уся райдужна оболонка або її частини можуть набувати більш коричневого кольору. У пацієнтів з однорідними блакитними, сірими, зеленими або карими очима протягом двох років лікування у клінічних випробуваннях з латанопростом зміна пігментації радужки спостерігались дуже рідко.
Зміни у кольорі райдужної оболонки виникають повільно, можуть залишатись непомітними від декількох місяців до років і не були пов’язані з будь-яким симптомом або паталогічними змінами.
Після припинення лікування подальше посилення коричневої пігментації райдужної оболонки не спостерігалося, однак наявна зміна кольору може залишитись постійною.
При наявності невусів або веснянок на райдужній оболонці не відзначалося їх зміни під впливом терапії.
Не спостерігалося накопичення пігменту у трабекулярній сітці або у будь-якому іншому відділі передньої камери ока, однак пацієнтам слід проходити регулярні обстеження та, якщо клінічна ситуація того вимагатиме, припинити лікування препаратом у випадку посилення пігментації райдужної оболонки.
На початку лікування слід проінформувати пацієнта про можливість зміни кольору очей. Лікування лише одного ока може призвести до перманентної гетерохромії.
Зміни в повіках і віях.
При використанні латанопросту повідомлялось про потемніння шкіри повік, яке зазвичай є оборотним.
Латанопрост може поступово змінювати вії та пушкове волосся навколо ока, в яке вводився препарат; до цих змін належать збільшення довжини, товщини, пігментації та кількості волосин у віях або пушковому волоссі, а також ріст вій у неправильному напрямку. Зміни у віях є оборотними та зникають після припинення застосування препарату.
Глаукома.
Відсутні документальні дані щодо досвіду застосування латанопросту при запальній, судинній або хронічній закритокутовій глаукомі, відкритокутовій глаукомі у пацієнтів з псевдофакією, а також при пігментній глаукомі. Латанопрост не впливає зовсім або незначно впливає на зіницю, проте дані про застосування препарату при гострих нападах закритокутової глаукоми відсутні. Тому застосовувати Фіксапрост при таких станах потрібно з обережністю.
Герпетичний кератит.
Латанопрост необхідно застосовувати з обережністю пацієнтам з герпетичним кератитом в анамнезі. Пацієнтам з активним кератитом, спричиненим вірусом простого герпесу, і пацієнтам з рецидивним герпетичним кератитом в анамнезі, особливо пов’язаним з аналогами простагландинів, застосування лікарського засобу слід уникати.
Макулярний набряк
Під час лікування латанопростом повідомлялося про макулярний набряк, включаючи цистоїдний макулярний набряк.
Такий набряк виникав в основному у пацієнтів з афакією, псевдофакією із розривом задньої капсули кришталика або передньої камери кришталика та у пацієнтів з наявними факторами ризику макулярного набряку. Таким пацієнтам Фіксапрост слід застосовувати з обережністю.
Допоміжні речовини
Фіксапрост містить олію рицинову поліетоксильовану, гідрогенізовану, що може спричинити шкірні реакції. На сьогодні не існує адекватних даних з безпеки стосовно цієї допоміжної речовини.
Застосування у період вагітності або годування груддю.
Вагітність.
Фіксапрост не застосовується у період вагітності.
Латанопрост.
Відсутні достатні дані щодо застосування латанопросту вагітним жінкам. Випробування з тваринами виявили репродуктивну токсичність. Потенціальний ризик для людей невідомий.
Тимолол.
Відсутні достатні дані щодо застосування тимололу вагітним жінкам. Тимолол не слід застосовувати під час вагітності, якщо це не є життєво необхідним. Для зменшення системного всмоктування див. розділ «Спосіб застосування та дози».
Епідеміологічні дослідження не виявили жодних тератогенних ефектів, але продемонстрували ризик виникнення затримки внутрішньоутробного розвитку плода при пероральному застосуванні бета-блокаторів. Також ознаки та симптоми блокади бета-адренорецепторів (наприклад, брадикардія, гіпотонія, респіраторний дистрес-синдром і гіпоглікемія) спостерігалися у дітей, народжених матерями, яким до пологів застосовували бета-блокатори. У разі застосування Фіксапросту до пологів необхідно ретельно контролювати стан новонародженої дитини протягом перших днів життя.
Період годування груддю.
Фіксапрост не застосовується жінкам, які годують груддю.
Тимолол.
Бета-блокатори екскретуються у грудне молоко. Проте, навіть при застосуванні терапевтичних доз тимололу у вигляді очних крапель, дуже малоймовірно, що його концентрація в молоці буде достатньою для проявів клінічних симптомів у дітей раннього віку. Щодо зменшення системного всмоктування див. розділ «Спосіб застосування та дози».
Латанопрост.
Латанопрост і його метаболіти можуть попадати у грудне молоко.
Репродуктивна функція.
У дослідах на тваринах не виявлено жодного впливу латанопросту і тимололу на репродуктивну функцію чоловіків і жінок.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами.
Лікарський засіб чинить незначний вплив на здатність керувати автотранспортом або іншими механізмами.
Закапування очних крапель може спричинити короткочасне затуманення зору. Необхідно зачекати до зникнення таких проявів і тільки після цього продовжити керувати автотранспортом або працювати з механізмами.
Спосіб застосування та дози.
Для офтальмологічного застосування.
Дозування.
Дорослі (в тому числі пацієнти літнього віку).
Рекомендується застосовувати лікарський засіб по 1 краплі в уражене око (очі) 1 раз на добу.
Якщо введення дози було пропущено, лікування слід продовжувати із наступної дози, як було заплановано. Максимальна добова доза не повинна перевищувати 1 краплю в уражене око (очі) 1 раз на добу.
Спосіб застосування
Як і при застосуванні будь-яких очних крапель, з метою зменшення можливої системної абсорбції рекомендується впродовж 2 хвилин стискати слізний мішок у ділянці медіального кута ока (оклюзія слізного канальця). Це необхідно робити одразу ж після закапування кожної краплі.
Перед закапуванням крапель очних слід знімати контактні лінзи. Встановлювати їх знову можна через 15 хвилин.
При застосуванні кількох офтальмологічних засобів місцевої дії препарати слід застосовувати з інтервалом щонайменше 5 хвилин.
Однодозовий контейнер містить достатню кількість розчину для лікування обох очей і призначений лише для одноразового використання.
Цей лікарський засіб є стерильним розчином, що не містить консервантів. Розчин із індивідуального однодозового контейнера має використовуватись для закапування в уражене око (очі) одразу після відкривання. Оскільки стерильність не зберігається після відкривання окремого однодозового контейнера, необхідно утилізувати контейнер з будь-яким залишком одразу після застосування.
Пацієнти повинні:
- запобігати контакту наконечника крапельниці із оком або повікою;
- використовувати розчин крапель очних одразу після першого відкривання однодозового контейнера і утилізувати контейнер із залишками препарату після застосування;
- ще не використані однодозові контейнери до застосування зберігати у саше.
Метод застосування
1. Вимийте руки та прийміть зручне положення сидячи або стоячи.
2. Відкрийте саше, що містить 5 однодозових контейнерів. Запишіть дату першого відкриття саше.
3. Від’єднайте один однодозовий контейнер від стрічки.
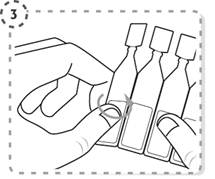
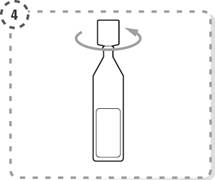
4. Відокремте верхню частину однодозового контейнера, як це зображено на малюнку. Не торкайтесь наконечника після відкриття контейнера.
5. За допомогою пальця обережно притисніть та відтягніть нижню повіку ураженого ока.
6. Розмістіть наконечник однодозового контейнера близько до ока, але не торкаючись його.
7. Стисніть обережно однодозовий контейнер таким чином, щоб в око потрапила лише одна крапля, потім відпустіть нижню повіку.

8. Притисніть пальцем внутрішній кут ураженого ока біля носа. Закрийте око і утримуйте притиснений палець впродовж 2 хвилин для зменшення можливої системної абсорбції. Це необхідно робити одразу ж після закапування кожної краплі.

9. Повторіть для іншого ока, якщо це призначено лікарем. Кожен однодозовий контейнер містить достатньо розчину для застосування для обох очей.
10. Утилізуйте однодозовий контейнер після використання. Не зберігайте для подальшого використання! Оскільки стерильність не може бути забезпечена після відкривання окремого однодозового контейнера, перед кожним застосуванням відкривають новий контейнер.
11. Інші однодозові контейнери, що залишились невикористаними, поміщають знову в саше. Саше, контейнери з якого почали застосовувати, знову поміщають в картонну коробку. Такі дії повторюють до закінчення контейнерів у саше або терміну їх використання. Контейнери з відкритого саше мають бути використані впродовж 1 місяця з дати його відкривання.
Діти.
Не застосовують. Безпека і ефективність лікарського засобу Фіксапрост для дітей і підлітків не встановлена.
Передозування.
Немає даних щодо передозування лікарського засобу Фіксапрост при його застосуванні відповідно до терапевтичних рекомендацій.
Симптоми.
Симптоми системного передозування тимололу: брадикардія, гіпотензія, бронхоспазм, можлива зупинка серця.
Окрім подразнення ока та кон’юнктивальної гіперемії, інших побічних ефектів з боку очей при передозуванні латанопросту не зафіксовано.
Лікування.
У випадку передозування застосовують симптоматичне і підтримувальне лікування.
Нижченаведена інформація може бути корисною у разі випадкового проковтування лікарського засобу.
Дослідження показали, що тимолол повільно виводиться зі шлунка. Тому, за необхідності, промивають шлунок.
Латанопрост в значною мірою метаболізується під час першого проходження через печінку. Внутрішньовенна інфузія препарату у дозі 3 мкг/кг здоровим добровольцям не спричиняла появи жодних симптомів, однак у дозі 5,5-10 мкг/кг спричиняла нудоту, біль у животі, запаморочення, підвищену втомлюваність, припливи та пітливість. Ці симптоми були від легкого до середнього ступеня тяжкості та пройшли без лікування протягом 4 годин після закінчення інфузії.
Побічні реакції.
Більшість побічних реакцій латанопросту — це порушення збоку органів зору. За даними розширеної фази основних випробувань референтного комбінованого препарату латанопрост/тимолол із вмістом консерванту, у 16-20 % пацієнтів спостерігається підвищена пігментація райдужної оболонки, що може бути необоротною. У відкритому 5-річному дослідженні з безпеки латанопросту у 33 % пацієнтів розвинулася пігментація райдужки (див. розділ «Особливості застосування»). Інші очні побічні реакції, як правило, є тимчасовими та виникають при застосуванні дози.
Найсерйозніші побічні реакції тимололу мають системний характер і включають брадикардію, аритмію, застійну серцеву недостатність, бронхоспазм та алергічні реакції.
Як і інші офтальмологічні препарати, що застосовуються місцево, тимолол всмоктується в системний кровотік. Це може спричинити побічні реакції, подібні до таких при застосуванні системних бета-блокаторів. Частота системних побічних реакцій після місцевого офтальмологічного застосування нижча, ніж при системному введенні. Перелічені побічні реакції включають реакції, що спостерігаються в групі офтальмологічних бета-блокаторів.
Побічні реакції, пов’язані з лікуванням, що спостерігались у клінічних випробуваннях із комбінованим референтним препаратом латанопрост/тимолол із вмістом консерванту, наведені нижче.
Таблиця 1. Побічні реакції, що спостерігались у клінічних випробуванняхлатанопросту/тимололу
Системи органів | Дуже часто (≥1/10) | Часто (≥1/100, <1/10) | Нечасто (≥1/1000, <1/100) |
З боку нервової системи | Головний біль | ||
З боку органів зору | Посилена пігментація райдужної оболонки | Біль в очах, подразнення ока (в тому числі поколювання, печіння, свербіж, відчуття чужорідного тіла в оці) | Розлади з боку рогівки, кон’юнктивіт, блефарит, гіперемія очей, нечіткість зору, посилена сльозотеча |
З боку шкіри та підшкірних тканин | Висип, свербіж |
Дані про побічні реакції окремих компонентів лікарського засобу Фіксапрост отримані у клінічних дослідженнях, зі спонтанних повідомлень у постмаркетинговий період, а також з наукових публікацій.
Таблиця 2. Побічні реакції латанопросту
Системи органів | Побічна реакція |
Інфекційні та паразитарні захворювання | Герпетичний кератит |
З боку нервової системи | Запаморочення |
З боку органів зору | Зміни вій та пушкового волосся (збільшення довжини, товщини, пігментації і кількості вій); точковий кератит, періорбітальний набряк, ірит; увеїт; макулярний набряк, включаючи кістозний макулярний набряк; сухість очей; кератит; набряк рогівки; ерозії рогівки; трихіаз; кіста райдужної оболонки; фотофобія; періорбітальні зміни та зміни повік, що призводять до поглиблення складки повік; набряк повік; місцева шкірна реакція на повіках; псевдопемфігоїд очної кон’юнктиви; потемніння пальпебральної шкіри повік. |
З боку серця | Стенокардія, нестабільна стенокардія, серцебиття |
З боку дихальної системи, органів грудної клітки та середостіння | Ядуха, загострення бронхіальної астми, задишка |
З боку опорно-рухового апарату та сполучної тканини | Міалгія, артралгія |
Загальні розлади та порушення у місці уведення | Біль у грудях |
Таблиця 3.Побічні реакції тимололу малеат (офтальмологічне застосування)
Системи органів | Побічна реакція |
З боку імунної системи | Системні алергічні реакції, у тому числі анафілактична реакція, ангіоневротичний набряк, кропив’янка, локалізований та генералізований висип, свербіж |
З боку обміну речовин та харчування | Гіпоглікемія |
З боку психіки | Втрата пам’яті, безсоння, депресія, нічні жахи, галюцинації |
З боку нервової системи | Геморагічний інсульт, церебральна ішемія, запаморочення, посилення ознак і симптомів міастенії гравіс, парестезія, головний біль, непритомність |
З боку органів зору | Відшарування судинної оболонки ока після фільтраційної операції, ерозія рогівки, кератит, диплопія, зниження чутливості рогівки, ознаки та симптоми подразнення очей (наприклад, печіння, поколювання, свербіж, сльозотеча та почервоніння), сухість очей, птоз, блефарит, нечіткість зору |
З боку органів слуху та рівноваги | Дзвін у вухах |
З боку серця | Зупинка серця, серцева недостатність, атріовентрикулярна блокада, застійна серцева недостатність, біль у грудях, аритмія, брадикардія, набряки, прискорене серцебиття |
З боку судин | Відчуття холоду в кистях і стопах, артеріальна гіпотензія, феномен Рейно |
З боку дихальної системи, органів грудної клітки та середостіння | Бронхоспазм (переважно у пацієнтів із бронхоспастичними захворюваннями в анамнезі), кашель, дихальна недостатність |
З боку шлунково-кишкового тракту | Біль у животі, блювання, діарея, сухість у роті, дисгевзія (зміна смакових відчуттів), диспепсія, нудота |
З боку шкіри та підшкірних тканин | Висипання на шкірі, псоріатичне висипання, загострення псоріазу, алопеція |
З боку опорно-рухового апарату та сполучної тканини | Міалгія |
З боку статевих органів і молочної залози | Статева дисфункція, зниження статевого потягу (лібідо) |
Загальні розлади та порушення у місці уведення | Астенія, слабкість |
Повідомлення щодо можливих побічних реакцій
Повідомлення про підозрювані побічні реакції після реєстрації лікарського засобу має важливе значення. Це дозволяє здійснювати моніторинг співвідношення ризик/користь при застосуванні лікарського засобу. Кваліфікованим працівникам охорони здоров’я необхідно повідомляти про будь-які підозрювані небажані реакції. Інформацію щодо проявів побічних реакцій надсилати на адресу: info@regata.in.ua або за телефоном (044) 467-57-70 (цілодобово), 585-04-60.
Термін придатності.
2 роки.
Після відкриття саше використати однодозові контейнери впродовж 1 місяця.
Після відкриття однодозового контейнера використати одразу та утилізувати однодозовий контейнер після використання.
Невикористані однодозові контейнери зберігати у саше з метою захисту їх від світла.
Умови зберігання.
Лікарський засіб не вимагає особливих температурних умов зберігання.
Однодозові контейнери зберігають у саше з метою захисту від світла.
Зберігати у недоступному для дітей місці та поза полем зору дітей.
Упаковка.
По 0,2 мл в однодозовому контейнері; по 5 однодозових контейнерів, з’єднаних між собою у стрічку, у саше; по 6 або 18 саше (№ 30 або 90) у картонній коробці.
Категорія відпуску.За рецептом.
Виробник.
ЕКСЕЛВІЗІОН / EXCELVISION
Місцезнаходження виробника та його адреса місця провадження діяльності.
27 вул. де ла Ломбардьер, АННОНЕ, 07100, Франція /
27 rue de la Lombardiere, ANNONAY, 07100, France
Заявник.
Лаборатуар Теа / Laboratoires Thea
Місцезнаходження заявника.
12 вул. Луі Блеріо 63100 КЛЕРМОН-ФЕРРАН СЕДЕКС 2, Франція /
12 rue Louis Bleriot 63100 CLERMONT-FERRAND CEDEX 2, France

На сайті наведено виключно офіційні оновлені інструкції без перекладів та скорочень.
Інформація про лікарські засоби представлена на сайті для ознайомлення, не є приводом для самолікування та не є рекламою лікарських засобів.
 Важливо! До кожного лікарського засобу, який ви купуєте, обов’язково має додаватися інструкція про застосування лікарського засобу.
Важливо! До кожного лікарського засобу, який ви купуєте, обов’язково має додаватися інструкція про застосування лікарського засобу.
Тримайте всі інструкції до препаратів Домашньої аптечки під рукою – завантажуйте мобільний додаток Ліки Контроль БЕЗКОШТОВНО

