ЦИСАТРАКУРІЙ КАЛЦЕКС
МНН: Cisatracurium
 від 2 °С до 8 °С. Не заморожувати
від 2 °С до 8 °С. Не заморожувати 

ІНСТРУКЦІЯ
для медичного застосування лікарського засобу
ЦИСАТРАКУРІЙ КАЛЦЕКС
(CISATRACURIUM KALCEKS)
C клад:
діюча речовина: сisatracurium;
1 мл розчину містить цисатракурію 2 мг (у вигляді цисатракурію бесилату);
1 ампула по 2,5 мл містить цисатракурію 5 мг (у вигляді цисатракурію бесилату);
1 ампула по 5 мл містить цисатракурію 10 мг (у вигляді цисатракурію бесилату);
1 ампула по 10 мл містить цисатракурію 20 мг (у вигляді цисатракурію бесилату);
допоміжні речовини:розчин бензолсульфонової кислоти, вода для ін՚єкцій.
Лікарська формаРозчин для ін՚єкцій та інфузій.
Основні фізико-хімічні властивості:прозорий безбарвний або жовтуватого кольору розчин.
Фармакотерапевтична група
Міорелаксанти з периферичним механізмом дії, інші сполуки четвертинного амонію.Код АТС M03A C11.
Фармакологічні властивості
Цисатракурій – бензилізохіноліновий міорелаксант периферичної дії недеполяризуючого типу зі середньою тривалістю дії для внутрішнього застосування. Блокує н-холінорецептори кінцевих пластинок скелетних м’язових волокон і перешкоджає деполяризуючій дії ацетилхоліну, у результаті чого виникає пригнічення нервово-м’язової передачі на рівні постсинаптичної мембрани.
Клінічні дослідження за участю людей показали, що цисатракурій не пов’язаний із дозозалежним вивільненням гістаміну навіть при дозах до 8 x ED95 включно.
Цисатракурій зв’язується з холінергічними рецепторами на моторній кінцевій пластині, щоб антагонізувати дію ацетилхоліну, що призводить до конкурентного блокування нервово-м’язової передачі. Ця дія легко нейтралізується антихолінестеразними лікарськими засобами, такими як неостигмін або едрофоній.
ED95 (доза, необхідна для отримання 95 % депресії реакції смикання м’язаadductor pollicisу відповідь на стимуляцію ліктьового нерва) цисатракурію оцінюється як 0,05 мг/кг маси тіла під час опіоїдної анестезії (тіопентон/фентаніл/мідазолам).
ED95 цисатракурію у дітей під час анестезії галотаном становить 0,04 мг/кг.
Біотрансформація/виведення
Циcатракурій піддається деградації в організмі при фізіологічних значеннях pH і температури шляхом елімінації Хофмана (хімічний процес) з утворенням лауданозину і метаболітів моночетвертинного акрилату. Моночетвертинний акрилат гідролізується неспецифічними естеразами плазми з утворенням метаболіту моночетвертинного спирту. Елімінація цисатракурію в основному незалежна від органів, але печінка і нирки є основними шляхами кліренсу його метаболітів.
Ці метаболіти не мають міорелаксуючої активності.
Фармакокінетика у дорослих пацієнтів
Некомпартментальна фармакокінетика цисатракурію не залежить від дози у дослідженому діапазоні (від 0,1 до 0,2 мг/кг, тобто від 2 до 4 × ED95).
Популяційне фармакокінетичне моделювання підтверджує і розширює ці дані до 0,4 мг/кг (8 х ED95). Фармакокінетичні параметри після введення 0,1 мг/кг і 0,2 мг/кг доз цисатракурію здоровим дорослим пацієнтам наведені в таблиці 1.
Таблиця 1
Параметр | Діапазон середніх значень |
Кліренс | 4,7 - 5,7 мл/хв/кг |
Об’єм розподілу в стійкому стані | 121 - 161 мл/кг |
Період напіввиведення | 22 - 29 хв |
Особливі групи пацієнтів
Фармакокінетика у літніх пацієнтів
Клінічно значущих відмінностей у фармакокінетиці цисатракурію у літніх і молодих дорослих пацієнтів немає. Профіль відновлення також не змінюється.
Фармакокінетика у пацієнтів з нирковою/печінковою недостатністю
Клінічно значущих відмінностей у фармакокінетиці цисатракурію у пацієнтів з термінальною стадією ниркової недостатності або термінальною стадією захворювання печінки і у здорових дорослих пацієнтів не спостерігалося. Їх профіль відновлення також не змінювався.
Фармакокінетика при введенні у вигляді інфузії
Фармакокінетика цисатракурію після інфузії не відрізняється від такої після одноразової болюсної ін’єкції. Профіль відновлення після інфузії цисатракурію не залежить від тривалості інфузії й аналогічний такому після одноразової болюсної ін’єкції.
Фармакокінетика у пацієнтів відділення інтенсивної терапії (ВІТ)
Фармакокінетика цисатракурію у пацієнтів ВІТ, які отримують тривалі інфузії, подібна до такої у здорових хірургічних дорослих, які отримують інфузії або одноразові болюсні ін’єкції. Профіль відновлення після інфузій цисатракурію у пацієнтів ВІТ не залежить від тривалості інфузії.
Концентрації метаболітів вище у пацієнтів ВІТ з порушеннями функції нирок і/або печінки (див. розділ «Особливості застосування»). Ці метаболіти не впливають на нервово-м’язову блокаду.
Клінічні характеристики
Показання.
Цисатракурій Калцекс показаний для застосування під час хірургічних та інших процедур у дорослих і дітей віком від 1 місяця. Також показанийдля застосування дорослим у відділенні інтенсивної терапії (ВІТ).
Можна використовувати як доповнення до загальної анестезії або седації у ВІТ для розслаблення скелетної мускулатури, а також для полегшення інтубації трахеї та штучної вентиляції легенів.
Протипоказання.
Підвищена чутливість до цисатракурію, атракурію або бензолсульфонової кислоти.
Взаємодія з іншими лікарськими засобами та інші види взаємодій.
Було показано, що багато лікарських засобів впливають на силу та/або тривалість дії недеполяризуючих нервово-м’язових блокаторів, зокрема:
Посилення дії
- Анестезуючі засоби, такі як енфлюран, ізофлуран, галотан (див. розділ «Спосіб застосування та дози») та кетамін;
- інші недеполяризуючі нервово-м’язові блокатори;
- інші лікарські засоби, такі як антибіотики (включаючи аміноглікозиди, поліміксини, спектриноміцин, тетрацикліни, лінкоміцин та кліндаміцин);
- антиаритмічні лікарські засоби (включаючи пропранолол, блокатори кальцієвих каналів, лідокаїн, прокаїнамід та хінідин);
- діуретики (включаючи фуросемід та, можливо, тіазиди, маніт та ацетазоламід);
- солі магнію та літію;
- гангліоблокатори (триметафан, гексаметоній).
У рідкісних випадках деякі лікарські засоби можуть погіршувати або виявляти приховану міастенію або фактично викликати міастенічний синдром, що в результаті може призвести до підвищеної чутливості до недеполяризуючих міорелаксантів. До таких лікарських засобів належать різні антибіотики, бета-блокатори (пропранолол, окспренолол), антиаритмічні засоби (прокаїнамід, хінідин), протиревматичні засоби (хлорохін, D-пеніциламін), триметафан, хлорпромазин, стероїди, фенітоїн і препарати літію.
Введення суксаметонію для пролонгування ефектів недеполяризуючих міорелаксантів може призвести до тривалої і складної блокади, яку важко усунути за допомогою антихолінестеразних засобів.
Послаблення дії
Зниження дії спостерігається після попереднього хронічного введення фенітоїну або карбамазепіну.
Застосування антихолінестеразних засобів зазвичай необхідне при лікуванні хвороби Альцгеймера (наприклад, донепезил), може скоротити тривалість і зменшити величину нервово-м’язової блокади, викликану цисатракурієм.
Дія відсутня
Попереднє введення суксаметонію не впливає на тривалість нервово-м’язової блокади після болюсних доз цисатракурію або на вимоги до швидкості інфузії.
Особливості застосування.
Попередження, що характеризують лікарський засіб
Цисатракурій паралізує дихальні м’язи, а також інші скелетні м’язи, але не впливає на свідомість або больовий поріг. Цисатракурій повинен вводитися тільки під наглядом анестезіологів або інших лікарів, які знайомі зі застосуванням і дією міорелаксантів. Повинно бути доступним обладнання для інтубації трахеї, а також для підтримки вентиляції легенів і адекватної артеріальної оксигенації.
Слід дотримуватися обережності при введенні цисатракурію пацієнтам, у яких була виявлена гіперчутливість до інших міорелаксантів, оскільки повідомлялося про високий ступінь перехресної чутливості (понад 50 %) серед міорелаксантів (див. розділ «Протипоказання»).
Цисатракурій не має значних ваголітичних або гангліоблокуючих властивостей. Отже, цисатракурій не робить клінічно значущого впливу на частоту серцевих скорочень і не усуває брадикардію, викликану багатьма анестетиками або стимуляцією блукаючого нерва під час операції.
Пацієнти з міастенією та іншими формами нервово-м’язових захворювань показали значну підвищену чутливість до недеполяризуючих міорелаксантів. Цим пацієнтам рекомендується початкова доза не більше 0,02 мг/кг.
Серйозні порушення кислотно-основного та/або сироваткового електролітного балансу можуть підвищити або знизити чутливість пацієнтів до міорелаксантів, які впливають на нервово-м’язову передачу.
Немає інформації про застосування цисатракурію новонародженим віком до одного місяця, оскільки його дія не було вивчена у цій групі пацієнтів.
Дія цисатракурію не було вивчена у пацієнтів зі злоякісною гіпертермією в анамнезі. Дослідження на чутливих до злоякісної гіпертермії свинях показали, що цисатракурій не викликає цей синдром.
Не було проведено досліджень цисатракурію у пацієнтів при операціях з індукованою гіпотермією (від 25 до 28 °C). Як і при застосуванні інших міорелаксантів, можна очікувати, що швидкість інфузії, необхідна для підтримки адекватної міорелаксації у цих умовах, буде значно знижена.
Дія цисатракурію не було вивчена у пацієнтів з опіками, однак, як і при застосуванні інших недеполяризуючих міорелаксантів, при введенні цисатракурію цим пацієнтам слід враховувати можливість збільшення необхідної дози і скорочення тривалості дії лікарського засобу.
Цисатракурій Калцекс є гіпотонічним розчином, тому його не слід вводити в одній інфузійній лінії з переливанням крові.
Пацієнти ВІТ
При введенні високих доз цього лікарського засобу лабораторним тваринам метаболіт цисатракурію та атракурію, лауданозин, асоціюється з тимчасовою гіпотензією, а у деяких видів – зі збудливою дією на мозок. У найбільш чутливих видів тварин ці ефекти виникали при концентраціях лауданозину в плазмі крові, аналогічних тим, які спостерігалися у деяких пацієнтів ВІТ після тривалої інфузії атракурію.
Оскільки при застосуванні цисатракурію швидкість інфузії нижче, концентрація лауданозину в плазмі крові становить приблизно третину від концентрації, що спостерігається після інфузії атракурію.
Були поодинокі повідомлення про судоми у пацієнтів ВІТ, які отримували атракурій та інші лікарські засоби. У цих пацієнтів зазвичай були один або кілька медичних станів, що призводили до судом (наприклад, черепно-мозкова травма, гіпоксична енцефалопатія, набряк мозку, вірусний енцефаліт, уремія). Причинно-наслідковий зв’язок із лауданозином не встановлений.
Застосування у період вагітності або годування груддю.
Вагітність
Адекватних даних про застосування цисатракурію вагітним немає. Дослідження на тваринах недостатні щодо впливу на вагітність, ембріональний розвиток/розвиток плода, пологи і постнатальний розвиток. Потенційний ризик для людини невідомий.
Цисатракурій Калцекс не слід застосовувати під час вагітності.
Період г одування груд дю
Невідомо, чи виділяється цисатракурію бесилат або його метаболіти в материнське молоко у людини.
Неможливо виключити ризик для дитини, яку годують груддю. Однак через короткий період напіввиведення не слід очікувати впливу на дитину,яку годують груддю, якщо мати відновитьгодування груддюпісля того, як дія речовини зникне. В якості запобіжного заходу годування груддю слід припинити під час лікування, а також рекомендується утриматися від наступного годування груддю протягом п’яти періодів напіввиведення цисатракурію, тобто приблизно протягом 3 годин після останньої дози або закінчення інфузії цисатракурію.
Фертильність
Дослідження фертильності не проводилися.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами.
Це застереження не стосується застосування лікарського засобу Цисатракурію Калцекс. Цисатракурій завжди застосовують у поєднанні зі загальною анестезією, тому в даному випадку застосовуються звичайні запобіжні заходи, пов’язані із виконанням завдань після загальної анестезії.
Спосіб застосування та дози.
Застосовують внутрішньовенно.
Цисатракурій повинен застосовуватися тільки під наглядом анестезіологів або інших лікарів, які знайомі з використанням і дією міорелаксантів. Повинні бути доступні засоби для інтубації трахеї, а також для підтримки вентиляції легенів і адекватної артеріальної оксигенації.
Цисатракурій Калцекс не слід змішувати в одному і тому ж шприці або вводити одночасно через одну і ту ж голку з емульсією пропофолу для ін’єкцій, або з лужними розчинами, такими як тіопентал натрію (див. розділ «Несумісність»).
Цисатракурій Калцекс не містить антимікробний консервант, тому призначений для застосування тільки одному пацієнтові.
Порада з контролю
Як і в разі застосування інших міорелаксантів, під час застосування цисатракурію рекомендується проводити моніторинг нейром’язової функції, щоб підібрати індивідуальне дозування.
Дозування
• Використання у вигляді внутрішньовенної болюсної ін’єкції.
Дозування для дорослих
Інтубація трахеї
Рекомендована інтубаційна доза цисатракурію для дорослих становить 0,15 мг/кг маси тіла. Ця доза створювала хороші або відмінні умови для інтубації трахеї через 120 секунд після введення цисатракурію після індукції анестезії пропофолом.
Більш високі дози скоротять час початку нервово-м’язової блокади.
У таблиці 2 наведені середні фармакодинамічні дані, коли цисатракурій вводили у дозах від 0,1 до 0,4 мг/кг маси тіла здоровим дорослим пацієнтам під час опіоїдної (тіопентал/фентаніл/мідазолам) анестезії чи анестезії пропофолом.
Таблиця 2
Середні фармакодинамічні дані після введення різноманітних доз цисатракурію
Початкова доза, мг/кг маси тіла | Попередній анестетик | Час до 90% супресії T1*, хв | Час до максимальної супресії T1*, хв | Час до 25% спонтаного відновлення T1*, хв |
0,1 | Опіоїд | 3,4 | 4,8 | 45 |
0,15 | Пропофол | 2,6 | 3,5 | 55 |
0,2 | Опіоїд | 2,4 | 2,9 | 65 |
0,4 | Опіоїд | 1,5 | 1,9 | 91 |
*T1 Реакція м’язуadductor pollicis на одиночний імпульс струму (сіпання), а також на перший компонент послідовності з чотирьох імпульсів після супрамаксимальної електричної стимуляції ліктьового нерва.
Анестезія енфлураном або ізофлураном може збільшити клінічно ефективну тривалість початкової дози цисатракурію на 15 %.
Підтримування
Нервово-м’язову блокаду можна продовжити за допомогою підтримуючих доз цисатракурію. Доза 0,03 мг/кг маси тіла забезпечує приблизно 20 хвилин додаткової клінічно ефективної нервово-м’язової блокади під час анестезії опіоїдом або пропофолом.
Послідовні підтримуючі дози не призводять до наростаючого подовження дії.
Спонтанне відновлення
Після початку спонтанного відновлення нервово-м’язової блокади його швидкість не залежить від введеної дози цисатракурію. Під час анестезії опіоїдом або пропофолом середній час відновлення від 25 % до 75 % і від 5 % до 95 % становить приблизно 13 і 30 хвилин відповідно.
Оборотність
Нервово-м’язова блокада після введення цисатракурію легко оборотна при застосуванні стандартних доз антихолінестеразних засобів. Середній час відновлення від 25 % до 75 % і до повного клінічного відновлення (співвідношення Т4: Т1 ≥0,7) становить приблизно 4 і 9 хвилин відповідно, після введення лікарського засобу для скасування блокуючого дії, в середньому при 10 % відновленні T1.
Дозування пацієнтам дитячого віку
Інтубація трахеї (педіатричні пацієнти віком від 1 місяця до 12 років)
Як і удорослих, рекомендована дляінтубаціїдозацисатракуріюстановить 0,15мг/кг маситіла,щовводитьсяшвидкопротягом5 – 10 секунд.
Ця доза створює хороші або відмінні умови для інтубації трахеї через 120 секунд після введення цисатракурію. Фармакодинамічні дані для цієї дози представлені в таблицях 3-5.
Дію цисатракурію не було вивчено для інтубації трахеї у педіатричних пацієнтів класу III-IV ASA (American Society of Anesthesiologists – Американське товариство анестезіологів). Є обмежені дані щодо застосування цисатракурію дітям віком до 2 років, які перенесли тривалу або серйозну операцію.
У педіатричних пацієнтів віком від 1 місяця до 12 років цисатракурій має коротшу клінічно ефективну тривалість і швидший профіль самовільного відновлення, порівняно з дорослими, при аналогічних умовах анестезії. Невеликі відмінності у фармакодинамічному профілі спостерігалися у дітей віком від 1 до 11 місяців та у дітей віком від 1 до 12 років, які узагальнені в таблиці 3 і таблиці 4.
Таблиця 3
Діти віком від 1 до 11 місяців
Доза цисатракурію, мг/кг маси тіла | Попередній анестетик | Час до 90% супресії T1*, хв | Час до максимальної супресії T1*, хв | Час до 25% спонтаного відновлення T1*, хв |
0,15 | Галотан | 1,4 | 2,0 | 52 |
0,15 | Опіоїд | 1,4 | 1,9 | 47 |
Таблиця 4
Діти віком від 1 до 12 років
Доза цисатракурію, мг/кг маси тіла | Попередній анестетик | Час до 90% супресії T1*, хв | Час до максимальної супресії T1*, хв | Час до 25% спонтаного відновлення T1*, хв |
0,15 | Галотан | 2,3 | 3,0 | 43 |
0,15 | Опіоїд | 2,6 | 3,6 | 38 |
Якщо цисатракурій не потрібний для інтубації: можна застосовувати дозу менше 0,15 мг/кг. Фармакодинамічні дані для доз 0,08 мг/кг і 0,1 мг/кг для дітей віком від 2 до 12 років представлені в таблиці 5.
Таблиця 5
Діти віком від 2 до 12 років
Доза цисатракурію, мг/кг маси тіла | Попередній анестетик | Час до 90% супресії T1*, хв | Час до максимальної супресії T1*, хв | Час до 25% спонтаного відновлення T1*, хв |
0,08 | Галотан | 1,7 | 2,5 | 31 |
0,1 | Опіоїд | 1,7 | 2,8 | 28 |
Застосування цисатракурію після суксаметонію у дітей не вивчалось (див. розділ «Взаємодія з іншими лікарськими засобами та інші види взаємодії»).
Можна очікувати, що галотан продовжить клінічно ефективну тривалість дії дози цисатракурію до 20 %. Немає інформації про застосування цисатракурію дітям під час анестезії іншими галогенованими фторвуглецевими анестетиками, але можна очікувати, що ці лікарські засоби також можуть продовжити клінічно ефективну тривалість дії дози цисатракурію.
Підтримування (педіатричні пацієнти віком від 2 до 12 років)
Нервово-м’язову блокаду можна продовжити за допомогою підтримуючих доз цисатракурію.
У дітей віком від 2 до 12 років доза 0,02 мг/кг маса тіла забезпечує приблизно 9 хвилин додаткової клінічно ефективної нервово-м’язової блокади під час анестезії галотаном. Послідовні підтримуючі дози не призводять до наростаючого подовження дії.
Недостатньо даних для складання конкретної рекомендації щодо підтримуючого дозування дітям віком до 2 років. Однак дуже обмежені дані клінічних досліджень дітей віком до 2 років дають підстави припустити, що підтримуюча доза 0,03 мг/кг може продовжити клінічно ефективну нервово-м’язову блокаду до 25 хвилин під час анестезії опіоїдом.
Спонтанне відновлення
Після початку спонтанного відновлення нервово-м’язової блокади, його швидкість не залежить від введеної дози цисатракурію. Під час анестезії опіоїдом або галотаном середній період відновлення від 25 % до 75 % і від 5 % до 95 % становить приблизно 11 і 28 хвилин відповідно.
Оборотність
Нервово-м’язова блокада після введення цисатракурію легко оборотна при застосуванні стандартних доз антихолінестеразних засобів. Середній період відновлення від 25 % до 75 % і до повного клінічного відновлення (відношення T4: T1 ≥0,7), після введення лікарського засобу для скасування блокуючої дії, становить приблизно 2 і 5 хвилин відповідно, в середньому при 13 % відновлення T1.
• Застосування у вигляді внутрішньовенної інфузії
Дозування дорослим і дітям віком від 2 до 12 років
Підтримка нервово-м’язової блокади може бути досягнута шляхом інфузії Цисатракурію Калцекс.
Рекомендується початкова швидкість інфузії 3 мкг/кг маси тіла/хв (0,18 мг/кг/год) для відновлення супресії T1 від 89 % до 99 % після появи ознак спонтанного відновлення. Після початкового періоду стабілізації міорелаксації швидкість від 1 до 2 мкг/кг маси тіла/хв (від 0,06 до 0,12 мг/кг/год) повинна бути достатньою для підтримки міорелаксації на цьому рівні у більшості пацієнтів.
Може знадобитися зниження швидкості інфузії до 40 %, якщо цисатракурій вводиться під час анестезії ізофлураном або енфлураном (див. розділ «Взаємодія з іншими лікарськими засобами та інші види взаємодій»).
Швидкість інфузії буде залежати від концентрації цисатракурію в розчині для інфузії, бажаного рівня нервово-м’язової блокади і маси тіла пацієнта. У таблиці 6 наведені рекомендації щодо застосування нерозбавленого розчину Цисатракурій Калцекс.
Таблиця 6
Швидкість введення розчину Цисатракурій Калцекс для інфузій
Маса тіла пацієнта, кг | Доза (мгк/кг/хв) | Швидкість інфузії | |||
1,0 | 1,5 | 2,0 | 3,0 | ||
20 | 0,6 | 0,9 | 1,2 | 1,8 | мл/год |
70 | 2,1 | 3,2 | 4,2 | 6,3 | мл/год |
100 | 3,0 | 4,5 | 6,0 | 9,0 | мл/год |
Безперервна інфузія цисатракурію з постійною швидкістю не пов’язана з наростаючим збільшенням або зменшенням міорелаксації.
Після припинення інфузії спонтанне відновлення нервово-м’язової блокади відбувається зі швидкістю, порівнянною зі швидкістю після одноразового болюсного введення.
• Дозування пацієнтам ВІТ.
Цисатракурій може вводитися шляхом болюсної ін’кції і/або інфузії дорослим пацієнтам ВІТ.
Початкова швидкість інфузії цисатракурію – 3 мкг/кг (маса тіла)/хв (0,18 мг/кг/год) – рекомендується для дорослих пацієнтів ВІТ. Можуть бути великі відмінності між пацієнтами щодо величини дози, доза може збільшуватися або знижуватися з часом. У клінічних дослідженнях середня швидкість інфузії складала 3 мкг/кг/хв [діапазон від 0,5 до 10,2 мкг/кг (маса тіла)/хв (від 0,03 до 0,6 мг/кг/год)].
Середній час до повного спонтанного відновлення після тривалої (до 6 днів) інфузії цисатракурію у пацієнтів ВІТ становив приблизно 50 хвилин.
Профіль відновлення після інфузій цисатракурію у пацієнтів ВІТ не залежить від тривалості інфузії.
Особливі групи пацієнтів
Дозування пацієнтам літнього віку
Літнім пацієнтам не потрібно змінювати дозування. У цих пацієнтів цисатракурій має фармакодинамічний профіль, подібний зі спостережуваним у молодих дорослих пацієнтів, але, як і у випадку інших міорелаксантів, його дія може початися трохи пізніше.
Дозування пацієнтам із нирковою недостатністю
Пацієнтам із нирковою недостатністю не потрібно змінювати дозування. У цих пацієнтів цисатракурій має подібний фармакодинамічний профіль, який спостерігався у пацієнтів з нормальною функцією нирок, але його дія може початися трохи пізніше.
Дозування пацієнтам із порушеннями функції печінки
Змін дозування не потрібно пацієнтам із термінальною стадією захворювання печінки. У цих пацієнтів цисатракурій має подібний фармакодинамічний профіль, який спостерігався у пацієнтів з нормальною функцією печінки, але його дія може початися трохи швидше.
Дозування пацієнтам зі серцево-судинними захворюваннями
При введенні шляхом швидкої болюсної ін’єкції (більше 5 – 10 секунд) дорослим пацієнтам зі серйозними серцево-судинними захворюваннями (Нью-Йоркська кардіологічна асоціація, клас I, III), які перенесли операцію зі шунтування коронарної артерії (CABG – Coronary Artery Bypass Surgery), введення цисатракурію не супроводжувалося клінічно значущою дією на серцево-судинну систему в будь-яких вивчених дозах (до 0,4 мг/кг включно (8 х ED95)). Проте існують обмежені дані щодо застосування доз понад 0,3 мг/кг для цієї групи пацієнтів.
Цисатракурій не вивчався у дітей, які перенесли операцію на серці.
Дозування новонародженим (віком до 1 місяця)
Застосування цисатракурію новонародженим не рекомендується, оскільки його застосування не було вивчено для цієї групи пацієнтів.
Вказівки до застосування
Лікарський засіб необхідно візуально перевірити перед застосуванням. Його не можна застосовувати, якщо є будь-які видимі ознаки погіршення якості (наприклад, наявність часток).
Як відкрити ампулу:
1) Повернути ампулу кольоровою точкою до себе. Злегка постукати пальцем по верхній частині ампули, щоб розчин опустився в нижню частину ампули
(Рис. 1).
2) Ампулу відкривати обома руками: утримуючи нижню частину ампули в одній руці, іншою рукою натиснути на верхню частину ампули в напрямку від кольорової точки (Рис. 2).
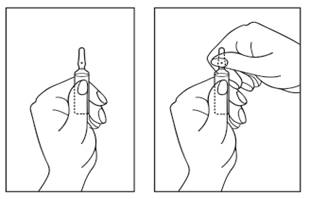
Рис. 1 Рис. 2
Розчин призначений тільки для одноразового застосування.
Лікарський засіб слід застосовувати відразу ж після розкриття ампули.
Розведений Цисатракурій Калцекс є фізично і хімічно стабільним протягом 24 годин при 2 – 8 °C і 25 °C у концентрації 0,1 мг/мл при контакті з поліпропіленовими або полікарбонатними шприцами, поліетиленовими або полівінілхлоридними (ПВХ) трубками і поліпропіленом або ПВХ інфузійними пакетами у таких інфузійних рідинах:
- розчин хлориду натрію 9 мг/мл (0,9 %) для ін’єкцій;
- розчин глюкози 50 мг/мл (5 %) для ін’єкцій;
- розчин хлориду натрію 1,8 мг/мл (0,18 %) і розчин глюкози 40 мг/мл (4 %) для ін’єкцій;
- розчин хлориду натрію 4,5 мг/мл (0,45 %) і розчин глюкози 25 мг/мл (2,5 %) для ін’єкцій.
Доведено, що цисатракурій сумісний з такими зазвичай використовуваними періопераційними засобами при змішуванні в умовах, що імітують введення в поточну внутрішньовенну інфузію через Y-подібний порт для ін’єкцій: альфентанілу гідрохлорид, дроперидол, фентанілу цитрат, мідазоламу гідрохлорид і суфентанілу цитрат.
Коли інші лікарські засоби вводяться через ту ж голку або канюлю, що і цисатракурій, рекомендується промивати їх достатнім обсягом рідини, що підходить для внутрішньовенного введення, наприклад розчином натрію хлориду 9 мг/мл (0,9 %) для ін’єкцій.
Як і при застосуванні інших лікарських засобів, що вводяться внутрішньовенно, коли в якості місця ін’єкції обрана невелика вена, цисатракурій слід вводити через вену разом із рідиною, придатною для внутрішньовенного введення, наприклад із розчином натрію хлориду 9 мг/мл (0,9 %) для ін’єкцій.
Діти.
Лікарський засіб показаний для застосування під час хірургічних та інших процедур дітям віком від 1 місяця. Застосування цисатракурію дітям віком до 1 місяця не рекомендується, оскільки його застосування не було вивчено для цієї категорії пацієнтів.
Передозування.
Симптоми і ознаки
Очікується, що основними симптомами передозування цисатракурію будуть тривалий параліч м'язів і його наслідки.
Лікування
Важливо підтримувати вентиляцію легенів і артеріальну оксигенацію, поки не відновиться адекватне спонтанне дихання. Буде потрібна повна седація, оскільки цисатракурій не порушує свідомість. Якщо є ознаки самовільного відновлення, воно може бути прискорене введенням антихолінестеразних засобів.
Побічні реакції.
Класифікація побічних реакцій за частотою розвитку: дуже часто (≥1/10), часто (від ≥1/100 до <1/10), нечасто (від ≥1/1000 до <1/100), рідко (від ≥1/10000 до <1/1000), дуже рідко (<1/10000).
З боку імунної системи: | |
Дуже рідко | Анафілактична реакція, анафілактичний шок. Анафілактичні реакції різного ступеня тяжкості спостерігалися після введення міорелаксантів, включаючи анафілактичний шок. Дуже рідко тяжкі анафілактичні реакції були зареєстровані у пацієнтів, які отримували цисатракурій у поєднанні з одним або з декількома анестетиками. |
З боку серця: | |
Часто | Брадикардія |
З боку судинної системи: | |
Часто | Гіпотензія. |
Нечасто | Почервоніння шкірних покривів. |
З боку дихальної системи, органів грудної клітки та середостіння : | |
Нечасто | Бронхоспазм |
З боку шкіри та підшкірних тканин: | |
Нечасто | Висипання |
З боку скелетно-м’язової та сполучної тканин: | |
Дуже рідко | Міопатія, м’язова слабкість |
Були окремі повідомлення про розвиток м’язової слабкості та/або міопатії після тривалого застосування міорелаксантів у тяжкохворих пацієнтів у відділенні інтенсивної терапії. Більшість пацієнтів отримували супутні кортикостероїди. Про такі випадки рідко повідомлялося у зв’язку із застосуванням цисатракурію, і причинно-наслідковий зв’язок не встановлений.
Термін придатності.
Нерозкриті ампули: 18 місяців.
Термін придатності після розведення
Після розведення не зберігати в холодильнику.
Хімічна та фізична стабільність після розведення була продемонстрована протягом 24 годин при температурі 2 – 8 °C та 25 °C.
З мікробіологічної точки зору, якщо метод розкриття/розведення не виключає ризик мікробного забруднення, лікарський засіб слід застосовувати негайно. Якщо він не застосовується негайно, то за час і умови зберігання до його застосування несе відповідальність користувач.
Не застосовувати після закінчення терміну придатності, зазначеного на упаковці.
Умови зберігання.
Зберігати та транспортувати в холодильнику при температурі від 2 °C до 8 °С. Не заморожувати. Зберігати в оригінальній упаковці для захисту від дії світла.
Зберігати в недоступному для дітей місці.
Несумісність.
Оскільки деградація цисатракурію бесилату відбувається значно швидше у розчині Рінгера лактату з 5 % декстрозою та у розчині Рінгера лактату, ніж у інших розчинниках, зазначених у розділі «Спосіб застосування та дози»,не рекомендується використовувати розчин Рінгера лактату з 5 % декстрозою та розчин Рінгера лактату як розчинники для приготування Цисатракурію Калцекс, розчину для інфузій.
Оскільки цисатракурію бесилат стабільний тільки у кислих розчинах, його не слід змішувати в одному і тому ж шприці або вводити одночасно через одну і ту ж голку з лужними розчинами (наприклад, тіопенталом натрію). Він також несумісний з ін’єкційною емульсією кеторолаку трометамолу або пропофолу.
Упаковка.
По 2,5 мл, 5 мл або 10 мл в ампулі із безкольорового скла І гідролітичного класу з маркувальними кільцями та з крапкою розламу.
По 5 ампул у контурній чарунковій упаковці із полівінілхлоридної плівки.
По 1 контурній чарунковій упаковці разом з інструкцією для медичного застосування в пачці з картону.
Категорія відпуску.
За рецептом.
Виробник.
Виробник, який відповідає за випуск серії:
АТ «Калцекс».
Місцезнаходження виробника та адреса місця провадження його діяльності.
Вул. Крустпілс, 71Е, Рига, LV-1057, Латвія.
Заявник.
АТ «Калцекс».
Місцезнаходження заявника.
Вул. Крустпілс, 53, Рига, LV-1057, Латвія.

На сайті наведено виключно офіційні оновлені інструкції без перекладів та скорочень.
Інформація про лікарські засоби представлена на сайті для ознайомлення, не є приводом для самолікування та не є рекламою лікарських засобів.
 Важливо! До кожного лікарського засобу, який ви купуєте, обов’язково має додаватися інструкція про застосування лікарського засобу.
Важливо! До кожного лікарського засобу, який ви купуєте, обов’язково має додаватися інструкція про застосування лікарського засобу.
Тримайте всі інструкції до препаратів Домашньої аптечки під рукою – завантажуйте мобільний додаток Ліки Контроль БЕЗКОШТОВНО

