ДИФЕРЕЛІН®
Зверніть увагу, якщо препарат було зареєстровано і виготовлено до дати закінчення реєстрації, він може продаватись.
дозволено до застосування в Україні, можуть застосовуватися в Україні до закінчення їх
терміну придатності, визначеного виробником та зазначеного на упаковці»
ст. 9 Закону України «Про лікарські засоби»
При зміні препарату обов’язково проконсультуйтесь з лікарем.

ІНСТРУКЦІЯ
для медичного застосування лікарського засобу
ДИФЕРЕЛІН®
( DIPHERELINE®)
Склад:
діюча речовина: трипторелін;
1 флакон містить триптореліну ацетат, що відповідає 3,75 мг триптореліну;
допоміжні речовини:D, L лактид когліколід полімер, маніт (Е 421), натрію кармелоза, полісорбат 80;
склад розчинника: 1 ампула містить маніт (Е 421), воду для ін’єкцій.
Порошок та розчинник для суспензії для ін’єкцій пролонгованого вивільнення.
Основні фізико-хімічні властивості:вміст флакона-майже білий ліофілізований порошок. Загальний вигляд відновленої суспензії-гомогенна молокоподібна суспензія.
Фармакотерапевтична група
Аналоги гонадотропін-рилізинг гормону. Код АТС L02A Е04.
Фармакологічні властивості
Трипторелін є синтетичним декапептидним аналогом гонадотропін-рилізинг гормону (ГнРГ). Дослідження на людях і на тваринах, показали, що після початкової стимуляції тривалий прийом триптореліну перешкоджає секреції гонадотропіну з подальшим пригніченням тестикулярної та оваріальної функцій.
Подальші дослідження на тваринах показали інший механізм дії-прямий вплив на гонади внаслідок зменшення чутливості периферійних рецепторів до ГнРГ.
Рак передміхурової залози
Введення добової дози триптореліну може спочатку підвищити рівні лютеїнізуючого гормону (ЛГ) та фолікулостимулюючого гормону (ФСГ) у крові та згодом призвести до підвищення первинного рівня тестостерону («спалах»). Продовження терапії знижує рівень ЛГ та ФСГ до концентрацій, які спричиняють зниження рівнів стероїдів до показників, що спостерігаються після кастрації, протягом 2-3 тижнів після ін’єкції та протягом усього періоду застосування лікарського засобу.
Терапія може підсилювати функціональні та об’єктивні симптоми.
У кількох рандомізованих довготривалих клінічних випробуваннях за участю пацієнтів з місцевопоширеним раком передміхурової залози доведено перевагу андроген-деприваційної терапії (АДТ) у поєднанні з радіотерапією (РТ) порівняно лише з РТ (RTOG 85-31, RTOG 86-10, EORTC 22863, D’Amico et al., JAMA, 2008).
У рандомізованому дослідженні фази ІІІ (EORTC 22961) за участю 970 пацієнтів з місцевопоширеним раком передміхурової залози (переважно T2c-T4 та декілька пацієнтів з раком Т1С-Т2В з патологічним реґіонарним нодальним ураженням) вивчали, чи променева терапія на тлі короткочасної антиандрогенної терапії (6 місяців, n = 483), не є гіршою за радіотерапію на тлі тривалої антиандрогенної терапії (3 роки, n = 487). Як агоністи ГнРГ застосовували трипторелін (62,2%) або інші агоністи ГнРГ. У дослідженні не проводили стратифікації за типом агоніста.
Загальна смертність протягом 5 років становила 19,0% та 15,2% відповідно в групах короткочасного гормонального лікування та тривалого гормонального лікування з відносним ризиком, що дорівнює 1,42 (ДІ 95,71% = 1,79; або 95,71% ДІ = [1,09; 1,85], p = 0,65-для оцінки неменшої ефективності та p = 0,0082-для оцінки різниці між групами за показниками дослідження заотриманими результатами). Смертність, пов’язана з раком передміхурової залози, протягом 5 років становила 4,78% та 3,2% відповідно в групах короткочасного гормонального лікування та тривалого гормонального лікування з відносним ризиком, що дорівнює 1,71 (ДІ 95% [1,14 до 2,57], p = 0,002). Загальна якість життя, яку оцінювали за допомогою опитувальника QLQ-C30, суттєво не відрізнялася у цих двох групах (Р = 0,37).
Аналіз отриманих результатів у підгрупі триптореліну також показав перевагу довготривалого лікування порівняно з короткостроковим лікуванням за показником загальної смертності (відносний ризик-1,28; ДІ 95,71% = [0,89; 1,84], p = 0,38 та p = 0,08 відповідно при дослідженні неменшої ефективності за отриманими результатами та для різниці між групами лікування).
Доказова база для застосування цього лікарського засобу при лікуванні високоризикованого локалізованого раку передміхурової залози спирається на опубліковані дані досліджень радіотерапії у поєднанні з терапією аналогами ГнРГ. Були проаналізовані клінічні дані п’яти досліджень (EORTC 22863, RTOG 85-31, RTOG 92-02, RTOG 86-10 та D’Amico et al., JAMA, 2008). Усі вони продемонстрували перевагу комбінування терапії аналогом ГнРГ та радіотерапії. Опубліковані дані досліджень не дозволяють провести чітку диференціацію відповідних популяцій за показаннями-місцевопоширений рак передміхурової залози та високоризикований локалізований рак передміхурової залози.
У пацієнтів з метастатичним кастраційно-резистентним раком передміхурової залози клінічні дослідження продемонстрували користь від додавання абіратерону ацетату як інгібітора біосинтезу андрогенів або ензалутаміду як інгібітора функції рецепторів андрогенів до аналогів ГнРГ, наприклад триптореліну.
Передчасне статеве дозрівання
Пригнічення гонадотропної гіперфункції гіпофіза в обох статей виражається пригніченням секреції естрадіолу та тестостерону, зниженням максимального значення ЛГ і покращенням показників «зріст-вік» та кісткового віку.
Початкова гонадна стимуляція може спричинити невелику кровотечу, при якій необхідним є застосування медроксипрогестерону або ципротерону ацетату.
Ендометріоз
Тривале лікування триптореліном пригнічує секрецію естрадіолу і таким чином забезпечує «спокій» ектопічного ендометрію.
Жіноче безпліддя
Тривала терапія триптореліном пригнічує секрецію гонадотропінів (ФСГ і ЛГ). Таким чином, терапія забезпечує пригнічення інтеркурентного ендогенного піка гормону ЛГ, уможливлюючи підвищення якості фолікулогенезу та прискорення відновлення фолікулів.
Фіброміоми матки
Проведені дослідження показали стійке та виражене зменшення в об’ємі фіброміом матки у певних випадках. Це зменшення досягає найвищого показника на третій місяць лікування.
Терапія триптореліном у більшості пацієнтів спричиняє аменорею після першого місяця терапії, що надає можливість скорегувати можливу анемію, яка виникає в результаті менорагії та/або метрорагії.
Рак молочної залози
Клінічні дослідження, проведені за участю жінок у передменопаузі з гормончутливим раком молочної залози на ранній стадії, передбачали застосування триптореліну з метою пригнічення секреції естрадіолу в яєчниках, де в основному виробляються естрогени. За результатами досліджень, проведених за участю здорових жінок і жінок з ендометріозом, ефект триптореліну досягається через 3-4 тижні після застосування.
У двох дослідженнях фази ІІІ (SOFT і TEXT) вивчали 5-річну перевагу терапії, спрямованої на пригнічення функції яєчників (OFS), у поєднанні з тамоксифеном (T) або інгібітором ароматази (екземестаном, E) у жінок у передменопаузі з гормончутливим раком молочної залози ранньої стадії.
Трипторелін був основним засобом лікування для досягнення OFS (91,0% рандомізованих пацієнток у дослідженні SOFT і 100%-у дослідженні TEXT). Решті 9% жінок у дослідженні SOFT провели двосторонню оваріектомію або двостороннє опромінення яєчників.
Результати дослідження SOFT
Дизайн дослідження SOFT мав на меті отримати відповіді на питання про додаткову цінність пригнічення функції яєчників при терапії тамоксифеном як ад'ювантній терапії жінок у передменопаузі з гормончутливим раком молочної залози ранньої стадії.
Загалом було проаналізовано дані 3047 жінок (1015 жінок в групі Т+OFS, 1018 жінок у групі монотерапії Т та 1014 жінок у групі Е+OFS).
При медіані періоду подальшого спостереження, що становила 67 місяців (5,6 року) лікування режимом Т+OFS несуттєво зменшило ризик безрецидивного виживання (DFS) порівняно з монотерапією Т (HR = 0,83; ДІ 95%, 0,66-1,04; p = 0,10). Розрахунковий 5-річний показник DFS становив 86,6% (ДІ 95%, 84,2-88,7%) у жінок в групі Т+OFS порівняно з 84,7% (ДІ 95%, 82,2-86,9%) у жінок в групі монотерапії T.
Однак після корегування на попередньо задані коваріати у багатофакторній моделі Кокса жінки, рандомізовані до групи Т+OFS, мали значно менший ризик події DFS порівняно з жінками, які отримували монотерапію Т. Зменшення становило 22% (HR = 0,78; ДІ 95%, 0,62-0,98; p = 0,03).
Жінки, яким призначили лікування режимом Т+OFS, мали незначною мірою зменшений ризик події раку молочної залози порівняно з жінками, які отримували монотерапію Т (HR = 0,81; ДІ 95%, 0,63-1,03; p = 0,09). Розрахунковий 5-річний інтервал без ознак раку молочної залози (BCFI) становив 88,4% (ДІ 95%, 86,1%-90,3%) у жінок, які отримували лікування режимом Т+OFS, порівняно з 86,4% (ДІ 95%, 84,0%-88,5%) у жінок, які отримували монотерапію Т.
Однак після корегування на попередньо задані коваріати у багатофакторній моделі Кокса жінки, рандомізовані до групи Т+OFS, мали значно зменшений ризик події BCFI порівняно з жінками в групі монотерапії Т. Зменшення ризику становило 25% (HR = 0,75; ДІ 95%, 0,59-0,96; p = 0,02).
Абсолютна перевага була вищою у жінок, які отримували ад'ювантну хіміотерапію. Показник 5-річного DFS у жінок, які проходили ад'ювантну хіміотерапію, становив 80,7% в групі T+OFS та 77,1% в групі монотерапії T (HR = 0,82; ДІ 95%, 0,64-1,07), при цьому абсолютна перевага становила 3,6% для режиму T+OFS.
Зокрема, користь від додавання OFS до схеми лікування була очевидною за 5-річним показником DFS за результатами аналізуpost hoc в підгрупі жінок віком до 40 років (HR = 0,74; ДІ 95%, 0,53, 1,03) з абсолютною перевагою на рівні 4,4% для режиму T+OFS порівняно з режимом монотерапії Т.
У дослідженні SOFT у пацієнток, яким призначили режим E+OFS, статистично достовірно зменшувався ризик події DFS порівняно з пацієнтками групи монотерапії Т (HR = 0,68, ДІ 95%, 0,53-0,86). Розрахунковий 5-річний показник DFS становив 89,0% (ДІ 95%, 86,8-90,9%) у пацієнток групи E+OFS порівняно з 84,7% (ДІ 95%, 82,2-86,9%) у пацієнток групи монотерапії Т.
У пацієнток, яким призначено режим E+OFS, спостерігали статистично достовірно зменшений ризик розвитку раку молочної залози порівняно з пацієнтками групи монотерапії Т (HR = 0,64; ДІ 95%, 0,49-0,83). Розрахунковий 5-річний показник BCFI становив 90,9% (ДІ 95%, 88,9-92,6%) у пацієнток групи E+OFS порівняно з 86,4% (ДІ 95%, 84,0-88,5%) у пацієнток, яким призначили монотерапію Т.
У пацієнток, яким призначено режим E+OFS, відмічали статистично достовірно зменшений ризик віддаленого рецидиву порівняно з пацієнтками групи монотерапії Т (HR = 0,71; ДІ 95%, 0,52-0,96). Розрахунковий 5-річний інтервал без віддалених рецидивів (DRFI) становив 93,0% (ДІ 95%, 91,2-94,5%) у суб'єктів, яким призначали режим E+OFS, порівняно з 90,7% (ДІ 95%, 88,6-92,4%).
Абсолютна перевага була вищою у жінок, які отримували ад'ювантну хіміотерапію. Показник 5-річного DFS у жінок, які проходили ад'ювантну хіміотерапію, становив 83,8% у групі E+OFS та 77,1% в групі монотерапії Т (HR = 0,70, ДІ 95%, 0,53-0,92) з абсолютною перевагою 6,7% для групи E+OFS.
Розрахунки DFS методом Каплана-Меєра у жінок, які отримували попередню хіміотерапію
Безрецидивна виживаність, попередня хіміотерапія |
Кількість років з моменту рандомізації Кількість пацієнтів в групі ризику |

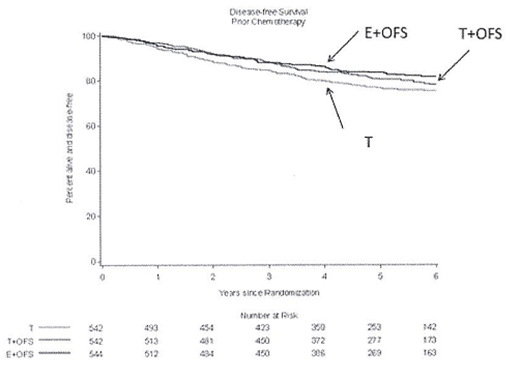
У дослідженні SOFT, що проводили в 3-х групах, жінки, які отримували хіміотерапію, мали більш високу частку клінічних критеріїв високого ризику рецидиву: 49,3% жінок віком < 40 років, 56,9% жінок з позитивними лімфатичними вузлами, 47,0% жінок з розміром пухлини молочної залози > 2 см і 33,7% з пухлиною 3 ступеня.
Сукупні результати досліджень SOFT та TEXT
Основна мета дослідження TEXT полягала в оцінці ролі інгібіторів ароматази (екземестану) при терапії OFS порівняно з режимом T+OFS у всіх учасниць досліджень SOFT і TEXT. Загалом проаналізовано дані 4690 жінок: 2346 жінок у групі Е+OFS та 2344 жінок у групі Т+OFS.
На момент досягнення медіани подальшого спостереження (68 місяців, 5,7 року) лікування режимом E+OFS статистично достовірно знижувало ризик події DFS порівняно з режимом T+OFS (HR = 0,72; ДІ 95%, 0,60-0,86; p = 0,0002). Розрахунковий 5-річний DFS становив 91,1% (ДІ 95%, 89,7-92,3%) у жінок, яким призначено режим E+OFS, у порівнянні з 87,3% (ДІ 95%, 85,7-88,7%) у жінок, яким призначено режим T+OFS.
Розрахунки показника DFS методом Каплана-Меєра в групах OFS+E та OFS+T
Кількість років з моменту рандомізації Кількість пацієнтів в групі ризику |

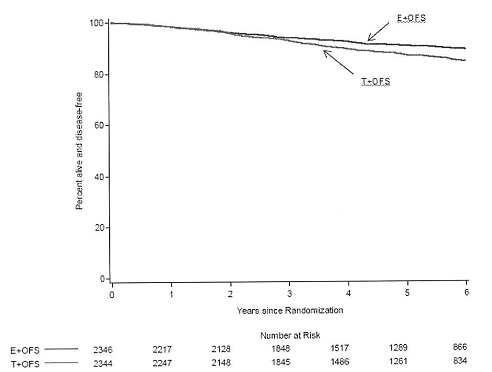
Жінки, яким призначали режим E+OFS, мали статистично достовірно зменшений ризик виникнення раку молочної залози порівняно з жінками, яким призначили режим T+OFS (HR = 0,66; ДІ 95%, 0,55-0,80; P <0,0001). Розрахунковий 5-річний показник BCFI покращився на рівні 92,8% (ДІ 95%, 91,6-93,9%) у жінок з режимом E+OFS, порівняно з 88,8% (ДІ 95%, 87,3-90,1%) у жінок, яким призначили режим T+OFS.
Після внутрішньом’язової ін’єкції цього лікарського засобу пролонгованого вивільнення спостерігається початкова фаза вивільнення активної речовини, після якої відбувається звичайне вивільнення протягом 28 днів.
Після внутрішньом’язової ін’єкції лікарського засобу Диферелін® (3,75 мг) у жінок з ендометріозом і фіброміомою матки максимальні рівні триптореліну в крові досягаються в інтервалі від 2 до 6 годин після ін’єкції, а пікове значення становить 11 нг/мл. Доказів накопичення лікарського засобу після щомісячних ін’єкцій протягом шести місяців не отримано.
Мінімальні концентрації у плазмі зберігалися в діапазоні від 0,1 та 0,2 нг/мл. Біодоступність лікарського засобу уповільненого вивільнення становить приблизно 50%.
Ці дані, які спостерігали у пацієнток з ендометріозом і фіброміомою матки, можна екстраполювати і на пацієнток з раком молочної залози, оскільки не очікується, що це захворювання матиме вплив на властивості цього лікарського засобу в лікарській формі пролонгованого вивільнення.
Клінічні характеристики
Показання.
· Рак передміхурової залози
Лікування високоризикованого локалізованого або місцевопоширеного раку передміхурової залози, у поєднанні з радіотерапією (див. розділ «Фармакодинаміка»).
Лікування місцевопоширеного або метастатичного раку передміхурової залози.
Сприятливий результат лікування є більш виражений та спостерігається частіше, якщо раніше пацієнт не отримував будь-якої іншої гормональної терапії.
· Передчасне статеве дозрівання у дітей (у дівчаток віком до 8 років та у хлопчиків віком до 10 років).
· Генітальний та екстрагенітальний ендометріоз (І-ІV стадій)
Терапію не проводити довше 6 місяців (див. розділ «Побічні реакції»). Проведення повторного курсу лікування триптореліном або іншим аналогом гонадотропін-рилізинг гормону (ГнРГ) не рекомендовано.
· Жіноче безпліддя
Додаткове лікування у поєднанні з гонадотропінами (менопаузальний гонадотропін людини (МГЛ), фолікулостимулюючий гормон (ФСГ), хоріонічний гонадотропін людини (ХГЛ)), для штучного відтворення умов овуляції з метою заплідненняin vitro і подальшої трансплантації ембріона (I.V.F.E.T).
· Лікування фіброміоми матки перед оперативним втручанням
- у зв’язку з анемією (рівень гемоглобіну нижче або дорівнює 8 г/дл);
- як допоміжний і коригуючий лікарський засіб при оперативному лікуванні у разі необхідності зменшення розміру фіброміоми: ендоскопічна операція, трансвагінальна операція.
Тривалість лікування обмежується трьома місяцями.
· Рак молочної залози
Як ад’ювантна терапія у поєднанні з тамоксифеном або інгібітором ароматази для лікування гормончутливого раку молочної залози ранньої стадії з високим ризиком рецидиву після завершення хіміотерапії у жінок з підтвердженим статусом передменопаузи (див. розділи «Протипоказання», «Особливості застосування», «Побічні реакції» та «Фармакодинамика»).
Протипоказання.
· Гіперчутливість до ГнРГ, його аналогів або до будь-яких допоміжних речовин цього лікарського засобу, вказаних у розділі «Склад» (див. розділ «Побічні реакції»).
· Період вагітності або годування груддю.
· Жінкам в передменопаузі, хворим на рак молочної залози: застосування інгібітора ароматази до досягнення у них адекватного пригнічення функції яєчників триптореліном (див. розділи «Спосіб застосування та дози» та «Особливості застосування»).
Суспензію для ін’єкцій слід розчиняти в асептичних умовах лише із застосуванням ампули з розчинником для ін’єкцій.
Слід чітко дотримуватися наступних інструкцій щодо приготування:
розчинник набрати у наданий шприц через голку для розчинення (20 G, без системи захисту) та перенести у флакон з порошком. Розчиняти, обережно струшуючи флакон, доки не утвориться однорідна суспензія молочного кольору. Флакон не перевертати.
Важливо перевірити відсутність агломератів порошку у флаконі. Після цього отриману суспензію набрати назад у шприц, не перевертаючи флакон. Після цього замінити голку для розчинення на голку для ін’єкцій (20 G, із системою захисту) для введення засобу.
Оскільки лікарський засіб має форму суспензії, ін’єкцію слід здійснити негайно після розчинення, щоб запобігти утворенню осаду.
Тільки для одноразового застосування.
Використані голки, будь-які рештки невикористаної суспензії або інші відходи необхідно утилізувати відповідно до місцевих вимог.
Взаємодія з іншими лікарськими засобами та інші види взаємодій
При застосуванні триптореліну з лікарськими засобами, які впливають на секрецію гіпофізарних гонадотропних гормонів, необхідно дотримуватися застережних заходів, а також рекомендований ретельний контроль за гормональним рівнем пацієнта.
Оскільки андроген-деприваційна терапія може подовжувати інтервал QT, одночасне застосування препарату Диферелін® (3,75 мг) з лікарськими засобами, які подовжують інтервал QT або здатні викликати шлуночкову тахікардію типу «пірует», такими як антиаритмічні засоби класу ІА (хінідин, дизопірамід тощо) або класу ІІІ (аміодарон, соталол, дофетилід, ібутилід), а також метадон, цизаприд, моксифлоксацин, антипсихотичні засоби, потребує ретельного оцінювання (див. розділ «Особливості застосування»).
Особливості застосування.
Застосування агоністів ГнРГ може викликати зниження мінеральної щільності кісткової тканини. Попередні дані показують, що у чоловіків застосування бісфосфонату разом з агоністом ГнРГ може знизити втрату мінералізації кісток. Особливу увагу необхідно приділяти пацієнтам з додатковими факторами ризику захворювання на остеопороз (такими як зловживання алкоголем, паління, тривале лікування засобами, які спричиняють зниження мінеральної щільності кісткової тканини, наприклад, протисудомними або кортикостероїдами, спадкова схильність до захворювання остеопорозом, недостатнє харчування).
До призначення Дифереліну® (3,75 мг) необхідно підтвердити відсутність у пацієнтки вагітності.
У рідкісних випадках терапія агоністами ГнРГ може виявити раніше не зафіксовану гонадотропну аденому гіпофіза. У таких пацієнтів може проявлятися гіпофізарна апоплексія, що характеризується раптовими головними болями, блюванням, порушеннями зору та офтальмоплегією.
Існує підвищений ризик розвитку депресії (що може бути тяжкою) у пацієнтів, що проходять лікування агоністами ГнРГ, зокрема триптореліном. З огляду на це пацієнтів потрібно відповідно інформувати та забезпечити належним лікуванням в разі появи симптомів. Пацієнти, що перебувають у стані депресії, потребують ретельного спостереження протягом терапії.
Диферелін® (3,75 мг) містить менше ніж 1 ммоль (23 мг) натрію на дозу, тобто загалом засіб вільний від натрію.
Слід з обережністю призначати цей лікарський засіб пацієнтам, які лікуються антикоагулянтами, через ризик виникнення гематом у місці ін’єкції.
Рак передміхурової залози
На початку терапія триптореліном, подібно до інших агоністів ГнРГ, призводить до тимчасового підвищення сироваткових рівнів тестостерону. В результаті протягом перших тижнів лікування можуть розвинутися поодинокі випадки тимчасового погіршення симптомів раку передміхурової залози. Протягом початкового етапу лікування слід розглянути можливість додаткового призначення відповідного антиандрогену для нейтралізації початкового збільшення рівня тестостерону в сироватці крові та попередження погіршення клінічних симптомів.
Незначна кількість пацієнтів може зазнати тимчасового погіршення симптомів раку передміхурової залози та тимчасового посилення болю, пов’язаного з раком (болю при метастатичному ураженні), що лікується симптоматично.
Як і у разі застосування інших агоністів ГнРГ, спостерігалися поодинокі випадки виникнення компресії спинного мозку або обструкції сечівника. У разі розвитку компресії спинного мозку чи порушення функції нирок застосовують стандартні методи лікування цих ускладнень, а в надзвичайних випадках розглядають можливість проведення негайної орхіектомії (хірургічної кастрації). Протягом перших тижнів лікування показаний ретельний моніторинг, особливо пацієнтів з вертебральними метастазами, з ризиком виникнення компресії спинного мозку та/або пацієнтів з обструкцією сечових шляхів. З тієї самої причини особливу обережність слід проявляти при призначенні лікування пацієнтам з продромальними ознаками компресії спинного мозку.
Після проведення хірургічної кастрації трипторелін не спричиняє в подальшому зниження рівня тестостерону в сироватці крові.
Тривала нестача андрогену внаслідок двобічної орхіектомії або введення аналогів ГнРГ підвищує ризик втрати кісткової маси та може призвести до захворювання на остеопороз, а також підвищує ризик перелому кісток.
Андроген-деприваційна терапія може спричинити подовження інтервалу QT.
Щодо пацієнтів з подовженням інтервалу QT в анамнезі або відповідними факторами ризику, а також у пацієнтів, що одночасно отримують лікарські засоби, які можуть подовжувати інтервал QT (див. розділ «Взаємодія з лікарськими засобами та інші види взаємодій»), лікарям слід оцінити співвідношення користі та ризику, зокрема потенційну можливість шлуночкової тахікардії типу «пірует», перш ніж призначати Диферелін® (3,75 мг).
До того ж, згідно з епідеміологічними даними, було визначено, що під час антиандрогенної терапії у пацієнтів можливі зміни в обміні речовин (наприклад порушення толерантності до глюкози) або підвищення ризику захворювань серцево-судинної системи. Хоча проспективні дані не підтвердили зв’язок між терапією аналогами ГнРГ і підвищенням летальності від серцево-судинних захворювань, пацієнти з високим ризиком порушення обміну речовин і серцево-судинних захворювань мають бути ретельно обстежені перед початком лікування і їм необхідно перебувати під належним наглядом протягом проведення антиандрогенної терапії.
У зв’язку з тривалою нестачею андрогену лікування аналогами ГнРГ може підвищити ризик анемії. Цей ризик потрібно оцінити та слід належним чином спостерігати за станом таких пацієнтів.
Введення триптореліну в лікарських дозах перешкоджає роботі гіпофізарно-гонадної системи. Як правило, її нормальне функціонування відновлюється після припинення терапії. Тому дані діагностичних тестів на функцію гіпофізарно-гонадної системи, які проводяться під час терапії аналогами ГнРГ та після її припинення, можуть бути хибними.
Можливе підвищення активності кислої фосфатази під час початкового періоду терапії.
Може бути корисним проведення періодичної перевірки рівня тестостерону в крові за допомогою точного методу, оскільки його показник не повинен перевищувати 1 нг/мл.
У жінок
Перед призначенням Дифереліну® (3,75 мг) потрібно переконатися, що пацієнтка не вагітна.
При використанні агоністів ГнРГ існує значний ризик зниження мінеральної щільності кісткової тканини, в середньому на 1% на місяць під час шестимісячного курсу терапії. Зниження мінеральної щільності кісткової тканини на 10% підвищує ризик переломів кісток у 2-3 рази.
Згідно з наявними даними, зниження кісткової щільності у більшості жінок припиняється після завершення терапії.
Наразі не існує конкретної інформації щодо пацієнток з виявленим остеопорозом або факторами ризику захворювання на остеопороз (наприклад, зловживання алкоголем, паління, тривале лікування засобами, які спричиняють зниження мінеральної щільності кісткової тканини, наприклад протисудомними або кортикостероїдами, спадкова схильність до захворювання на остеопороз, недостатнє харчування, наприклад нервово-психічна анорексія). Оскільки зниження мінералізації кісток може бути згубним для таких пацієнток, рішення про призначення триптореліну слід приймати індивідуально. Терапію можна розпочинати, лише якщо позитивний ефект перевищує ризик згідно з ретельно проведеною оцінкою. Необхідно приділити увагу додатковим заходам для протидії зниженню мінеральної щільності кісткової тканини.
· Жіноче безпліддя
Відновлення фолікулів може значно зрости внаслідок введення триптореліну разом з гонадотропними гормонами схильним до цього пацієнткам і особливо пацієнткам із синдромом полікістозу яєчників. Як і у разі застосування інших аналогів ГнРГ, було зафіксовано виникнення синдрому гіперстимуляції яєчників, пов’язаного з застосуванням триптореліну разом з гонадотропними гормонами.
Реакція яєчників на застосування триптореліну разом з гонадотропними гормонами може відрізнятися у різних пацієнток, які приймають однакову дозу, та в деяких випадках у однієї пацієнтки під час різних циклів.
Необхідне забезпечення пильного медичного нагляду при індукованій овуляції з проведенням точного та регулярного біологічного та клінічного контролю: експрес-тести на рівень естрогенів у плазмі крові, УЗД (див. розділ «Побічні реакції»).
При надмірній реакції яєчників рекомендовано перервати цикл стимуляції шляхом припинення введення гонадотропних гормонів.
У пацієнток з нирковою та печінковою недостатністю кінцевий період напіввиведення в середньому становить 7-8 годин, тоді як його середній показник у здорових жінок становить 3-5 годин. Незважаючи на таку тривалу дію, триптореліну вже не має бути в крові на момент пересадки ембріона.
· Ендометріоз і лікування фіброміоми матки перед оперативним втручанням
Регулярне застосування, кожні 4 тижні, одного флакона лікарського засобу Диферелін® (3,75 мг) спричиняє постійну гіпогонадотропну аменорею.
При виникненні генітальної кровотечі після першого місяця необхідно визначити рівень естрадіолу в плазмі крові. Якщо показник становить менше ніж 50 пг/мл, слід провести дослідження на можливе органічне ураження.
Оскільки менструація в період лікування триптореліном має припинитися, слід повідомити пацієнтку про необхідність проінформувати свого лікаря у разі продовження звичайного менструального циклу.
Під час проходження курсу терапії та протягом 1 місяця після введення останньої ін’єкції необхідно застосовувати негормональні методи контрацепції (див. розділ «Застосування у період вагітності або годування груддю»).
Після припинення терапії функція яєчників відновлюється і овуляція відбувається приблизно через 2 місяці після введення останньої ін’єкції.
При лікуванні маткових фіброїдів рекомендовано регулярно проводити дослідження розміру фіброїда. Було зафіксовано декілька випадків кровотечі у пацієнток з підслизовими фіброїдами при лікуванні аналогом ГнРГ. Як правило, кровотеча відбувається на 6-10-му тижні від початку лікування.
· Рак молочної залози
Для забезпечення адекватного пригнічення функції яєчників у жінок у передменопаузі лікування триптореліном призначають принаймні за 6-8 тижнів до початку терапії інгібітором ароматази. Щомісячні ін’єкції триптореліну слід проводити за графіком та без перерв увесь період терапії інгібітором ароматази.
У жінок у передменопаузі, яким діагностовано рак молочної залози і у яких після хіміотерапії припинилися менструації, виробництво яєчниками естрогену може зберігатися або не зберігатися. Незалежно від менструального статусу, необхідно підтвердити статус передменопаузи після хіміотерапії і до початку терапії триптореліном за рівнем концентрації естрадіолу та фолікулостимулюючого гормону (ФСГ) в крові відповідно до референтних значень для жінок в передменопаузі з метою уникнення небажаного лікування триптореліном при розвитку менопаузи на фоні хіміотерапії. Після початку лікування триптореліном важливо підтвердити адекватне пригнічення функції яєчників (менопаузи, індукованої аналогом гонадотропіну) шляхом проведення тестів на циркулюючий ФСГ та тестів на рівень естрадіолу з метою встановлення статусу істинної постменопаузи, якщо ця підгрупа жінок розглядається щодо лікування інгібітором ароматази відповідно до поточних рекомендацій клінічної практики. Відповідно, пригнічення функції яєчників має підтверджуватися низькими концентраціями ФСГ та естрадіолу в крові до початку лікування інгібітором ароматази. Тести повторюють кожні три місяці у період цієї комбінованої терапії триптореліном і інгібітором ароматази.
Ці заходи мають на меті уникнути «рикошетного» збільшення рівнів циркулюючого естрогену на тлі терапії інгібітором ароматази з відповідними наслідками для раку молочної залози. Слід зазначити, що рівні циркулюючого ФСГ знижуються у відповідь на індуковане аналогом гонадотропіну пригнічення функції яєчників (індуковану менопаузу), на відміну від природної менопаузи, при якій рівні ФСГ підвищуються.
Трипторелін при його застосуванні як ад’ювантної терапії у поєднанні з тамоксифеном або інгібітором ароматази пов’язують з високим ризиком остеопорозу. Про випадки остеопорозу частіше повідомляли після застосування триптореліну у поєднанні з інгібітором ароматази, аніж у поєднанні з тамоксифеном (39% порівняно з 25%).
Щільність кісткової маси слід оцінювати до початку терапії триптореліном, особливо у жінок з кількома факторами ризику розвитку остеопорозу. Слід забезпечити ретельний моніторинг стану цих пацієнтів, а за потреби - лікування або профілактику остеопорозу.
У жінок в передменопаузі лікування гормончутливого раку молочної залози ранньої стадії триптореліном у поєднанні з тамоксифеном або інгібітором ароматази слід проводити після ретельної індивідуальної оцінки ризиків і переваг.
Пацієнткам, яким відмінено лікування триптореліном, слід також відмінити терапію інгібіторами ароматази упродовж 1 місяця після останнього застосування триптореліну пролонгованого вивільнення.
При застосуванні триптореліну в поєднанні або з інгібітором ароматази, або тамоксифеном ризик розвитку порушень з боку скелетно-м’язової системи (включаючи біль у суглобах та скелетно-м’язовий біль) становить 89% на тлі інгібітора ароматази та приблизно 76% на тлі тамоксифену.
При застосуванні триптореліну у поєднанні або з екземестаном, або з тамоксифеном (див. розділ «Побічні реакції») повідомляли про артеріальну гіпертензію як про передбачуване побічне явище, що виникало дуже часто. У жінок в передменопаузі, хворих на рак молочної залози, які отримують трипторелін у поєднанні або з екземестаном, або з тамоксифеном, доцільно забезпечити регулярний моніторинг факторів ризику серцево-судинних порушень та кров’яного тиску.
При застосуванні триптореліну у поєднанні або з екземестаном, або з тамоксифеном (див. розділ «Побічні реакції») повідомляли про гіперглікемію та діабет, як про передбачуване побічне явище, що виникало часто. У жінок в передменопаузі, хворих на рак молочної залози, які отримують трипторелін у поєднанні або з екземестаном, або з тамоксифеном, доцільно забезпечити регулярний моніторинг факторів ризику діабету з регулярним моніторингом глюкози крові, а за потреби - призначити відповідну протидіабетичну терапію згідно з національними настановами.
Депресія виникала у приблизно 50% пацієнток, які отримували трипторелін у поєднанні або з тамоксифеном, або з екземестаном у всіх групах лікування досліджень TEXT та SOFT, однак у менше 5% пацієнток депресія була важкою (3-4 ступеня). Пацієнток слід поінформувати про це, а у разі появи симптомів-призначити відповідне лікування. Пацієнтки з діагностованою депресією або з депресією в анамнезі під час лікування мають перебувати під ретельним спостереженням.
Також слід уважно ознайомитися з інструкцією з медичного застосування екземестану та тамоксифену щодо відповідної інформації з безпеки застосування цих засобів у поєднанні з триптореліном.
Хіміотерапія може викликати тимчасову аменорею або перманентне припинення функції яєчників через цитотоксичне ураження гонадної тканини. Збереження статусу передменопаузи після завершення хіміотерапії слід підтвердити відповідно до клінічних рекомендації шляхом визначення концентрації естрадіолу та ФСГ у крові та порівняння отриманих значень із референтними для жінок у передменопаузі.
Передчасне статеве дозрівання
Лікування дітей з прогресуючою пухлиною головного мозку необхідно розпочинати після ретельної оцінки ризику та користі від лікування.
У дівчаток початкова гонадна стимуляція може спричинити протягом першого місяця вагінальну кровотечу слабкої або середньої інтенсивності.
Після завершення терапії відбувається розвиток характеристик статевого дозрівання.
Інформація про стан репродуктивної функції у дітей, які проходили лікування аналогами ГнРГ, обмежена. У більшості дівчаток регулярний менструальний цикл розпочинався в середньому через рік після припинення терапії.
Необхідно виключити можливість псевдопередчасного статевого дозрівання (гонадна пухлина та пухлина надниркової залози, а також гіперплазія) і гонадотропіннезалежного передчасного статевого дозрівання (тестикулярний токсикоз, родинна гіперплазія клітин Лейдіга).
Під час лікування передчасного статевого дозрівання центрального ґенезу агоністами ГнРГ може знижуватись мінеральна щільність кісткової тканини. Однак після припинення лікування відбувається подальше накопичення кісткової маси, а на максимальну кісткову масу у пізньому пубертатному періоді лікування не впливає.
Після припинення лікування агоністами ГнРГ може розвиватися зміщення епіфізу голівки стегна. Припускають, що низька концентрація естрогену під час лікування агоністами ГнРГ ослаблює епіфізарну пластинку. Прискорення росту після завершення лікування призводить до зменшення сили, необхідної для зміщення епіфізу.
Застосування у період вагітності або годування груддю.
Вагітність
Трипторелін не можна застосовувати під час вагітності, оскільки супутнє застосування агоністів ГнРГ пов’язане з теоретичним ризиком аборту чи вад розвитку у дитини. Перед початком лікування потенційно фертильним жінкам слід пройти ретельне обстеження, щоб виключити ймовірність вагітності. Під час лікування і до відновлення менструацій слід застосовувати негормональні методи контрацепції.
Перед призначенням Дифереліну® (3,75 мг), зокрема перед лікуванням від безпліддя, необхідно переконатися, що пацієнтка не вагітна.
У цієї категорії пацієнток немає клінічних доказів причинно-наслідкового зв’язку між застосуванням триптореліну і будь-яким подальшим атиповим розвитком ооцитів або вагітності чи її наслідку.
Годування груддю
Трипторелін протипоказано застосовувати у період годування груддю.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами.
Досліджень впливу на швидкість реакції при керуванні автотранспортом або іншими механізмами не проводилося. Проте здатність керувати транспортними засобами та працювати з іншими механізмами може бути ускладнена внаслідок запаморочення, сонливості та порушень зору, які є можливими небажаними ефектами терапії або результатом основного захворювання.
Спосіб застосування та дози
Дози
·Рак передміхурової залози
Одна внутрішньом’язова ін’єкція Диферелін® (3,75 мг) кожні 4 тижні.
Тривалість лікування
При лікуванні високоризикованого локалізованого або місцевопоширеного гормонзалежного раку передміхурової залози, коли лікарський засіб застосовують як супутню терапію та після радіотерапії, клінічні дані продемонстрували, що радіотерапія з подальшою довготривалою антиандрогенною терапією є більш прийнятною, ніж радіотерапія з подальшою короткостроковою антиандрогенною терапією (див. розділ «Фармакодинаміка»).
Тривалість антиандрогенної терапії, рекомендована медичними посібниками пацієнтам з високоризикованим локалізованим або місцевопоширеним раком передміхурової залози, які проходять радіотерапію, становить 2-3 роки.
Пацієнтам з метастатичним кастраційно-резистентним раком передміхурової залози, які не проходили хірургічну кастрацію та отримують агоніст ГнРГ, наприклад трипторелін, і для яких лікування абіратерону ацетатом як інгібітором біосинтезу андрогенів або ензалутамідом як інгібітором функції рецепторів андрогенів є прийнятним, терапію агоністом ГнРГ слід продовжувати.
·Передчасне статеве дозрівання
Лікування дітей триптореліном потрібно проводити під ретельним наглядом дитячого ендокринолога, педіатра або ендокринолога з досвідом лікування передчасного статевого дозрівання центрального ґенезу.
Діти з масою тіла до 20 кг: половина (1/2) дози внутрішньом’язово кожні 4 тижні (28 днів), тобто введення половини об’єму приготованої суспензії.
Діти з масою тіла від 20 до 30 кг: дві третини (2/3) дози внутрішньом’язово кожні 4 тижні (28 днів), тобто введення двох третин об’єму приготованої суспензії.
Діти з масою тіла більше 30 кг: 1 доза внутрішньом’язово кожні 4 тижні (28 днів), тобто введення повного об’єму приготованої суспензії.
·Ендометріоз
Одна внутрішньом’язова ін’єкція Диферелін® (3,75 мг) кожні 4 тижні.
Лікування необхідно розпочинати у перші п’ять днів менструального циклу.
Тривалість лікування залежить від початкового ступеня тяжкості ендометріозу та зменшення клінічних проявів (функціональних і анатомічних) під час лікування. Курс лікування ендометріозу має становити щонайменше 4 місяці і щонайбільше 6 місяців. Не рекомендовано розпочинати другий курс лікування триптореліном або іншим аналогом ГнРГ.
·Жіноче безпліддя
Звичайна терапевтична схема базується на застосуванні одного флакона Диферелін® (3,75 мг), який застосовують внутрішньом’язово на другий день менструального циклу. Поєднання з гонадотропінами слід розпочинати після досягнення гіпофізарної десенсибілізації (рівень плазмового естрогену не перевищує 50 пг/мл), зазвичай на 15-й день після ін’єкції Диферелін® (3,75 мг).
·Лікування фіброміоми матки перед оперативним втручанням
Одна внутрішньом’язова ін’єкція Диферелін® (3,75 мг) кожні 4 тижні.
Лікування необхідно розпочинати у перші п’ять днів менструального циклу.
Тривалість лікування обмежується 3 місяцями.
УВАГА! Важливо, щоб ін’єкція лікарського засобу пролонгованого вивільнення була виконана точно за рекомендаціями у інструкції для медичного застосування лікарського засобу. Кожну невдалу ін’єкцію, після якої у шприці залишається лікарського засобу більше, ніж передбачено інструкцією, необхідно реєструвати.
·Рак молочної залози
Одна внутрішньом’язова ін’єкція кожні 4 тижні в поєднанні з тамоксифеном або інгібітором ароматази.
Терапію триптореліном розпочинають після завершення хіміотерапії, відразу після підтвердження статусу передменопаузи (див. розділ «Особливості застосування»).
Лікування триптореліном обов’язково розпочинають щонайменше за 6-8 тижнів до початку лікування інгібітором ароматази. Перш ніж розпочинати лікування інгібітором ароматази необхідно провести щонайменше дві ін’єкції триптореліну (з інтервалом 4 тижні між ін’єкціями).
Під час лікування інгібітором ароматази терапію триптореліном переривати не можна з метою уникнення «рикошетного» підвищення рівнів циркулюючих естрогенів у жінок в передменопаузі.
Рекомендована тривалість лікування у разі ад’ювантної терапії разом з іншою гормонотерапією становить не більше 5 років.
Слід суворо уникати випадкових внутрішньосудинних ін’єкцій через те, що Диферелін® (3,75 мг) є мікросферичною суспензією для ін’єкцій.
НИЖЧЕНАВЕДЕНА ІНФОРМАЦІЯ ПРИЗНАЧЕНА ЛИШЕ ДЛЯ МЕДИЧНИХ ПРАЦІВНИКІВ
Інструкція з використання лікарського засобу
1. ПІДГОТОВКА ПАЦІЄНТА ПЕРЕД РОЗВЕДЕННЯМ ЛІКАРСЬКОГО ЗАСОБУ | |||||||
Завчасно продезінфікувати місце ін’єкції, оскільки лікарський засіб після розведення вводиться негайно. | |||||||
2. ПІДГОТОВКА ДО ІН’ЄКЦІЇ | |||||||
Коробка містить 2 голки: | |||||||
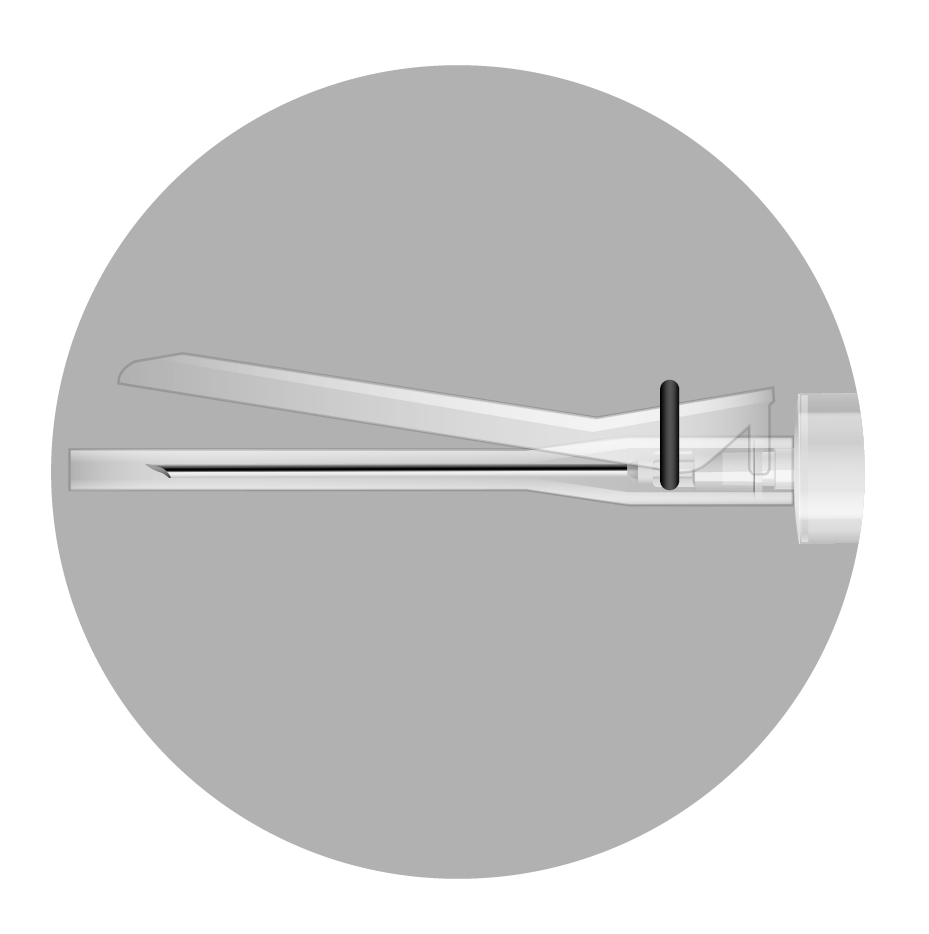
•Голка 1: довга голка (38 мм) без системи захисту для розведення порошку. •Голка 2: довга голка (38 мм) із системою захисту для виконання ін’єкції. | |||||||
| |||||||
Наявність бульбашок у верхній частині ліофілізату є нормальним зовнішнім виглядом лікарського засобу. | |||||||
2а - Вийняти ампулу з розчинником. У разі наявності розчину в шийці ампули постукати по ній, щоб увесь розчин перемістився в основну частину ампули. - Нагвинтити голку 1 (без системи захисту) на шприц, не знімаючи захисного ковпачка голки. - Відламати шийку ампули, тримаючи її точкою надлому до себе. - Зняти захисний ковпачок голки з голки 1. Вставити голку в ампулу і набрати увесь розчинник в шприц. - Відкласти в сторону шприц із розчинником. |
| ||||||
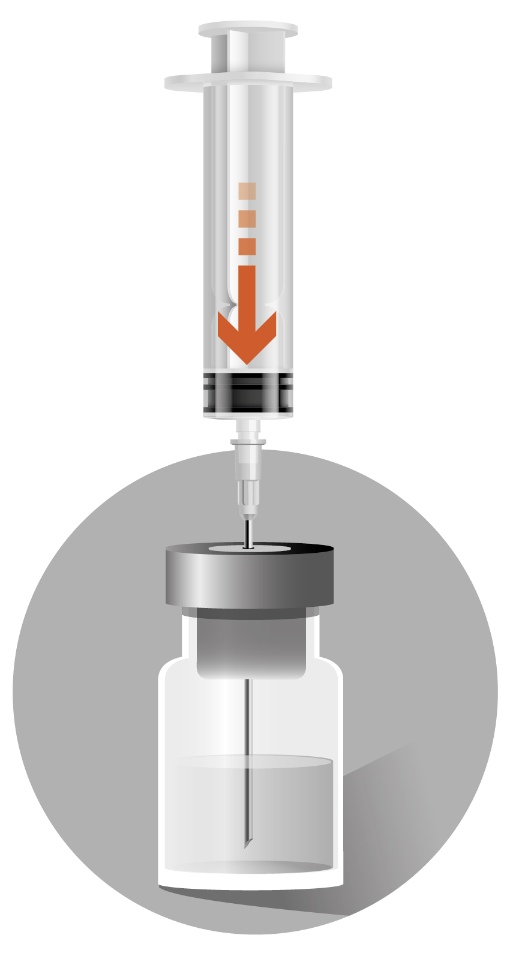
2б - Вийняти флакон із порошком. У разі наявності порошку у шийці флакона постукати по ній, щоб увесь порошок перемістився в нижню частину флакона. - Зняти пластиковий ковпачок у верхній частині флакона. - Взяти шприц з розчинником і проколоти голкою гумову пробку вертикально у флакон. - Повільно ввести розчинник, щоб, по можливості, обмити ним усю верхню частину флакона. |
| ||||||
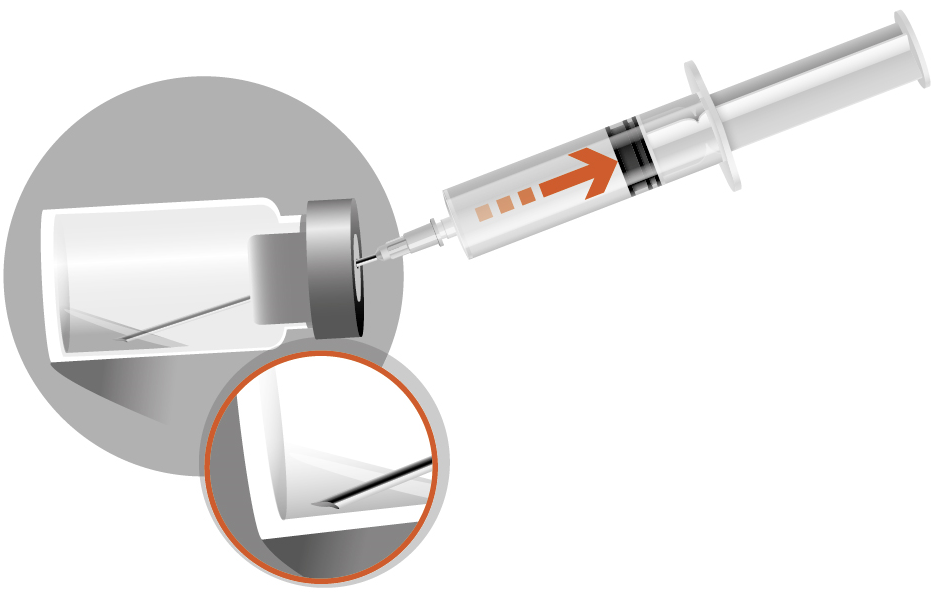
2в - Підняти голку 1 над рівнем рідини. Не виймати голку з флакона. Розвести суспензію шляхом легкого погойдування зі сторони в сторону. Не перевертати флакон. - Помішувати до отримання однорідної суспензії молочно-білого кольору. Важливо: переконатися у відсутності агломератів порошку у флаконі (при наявності грудочок порошку продовжувати перемішувати до їх зникнення). |
| ||||||
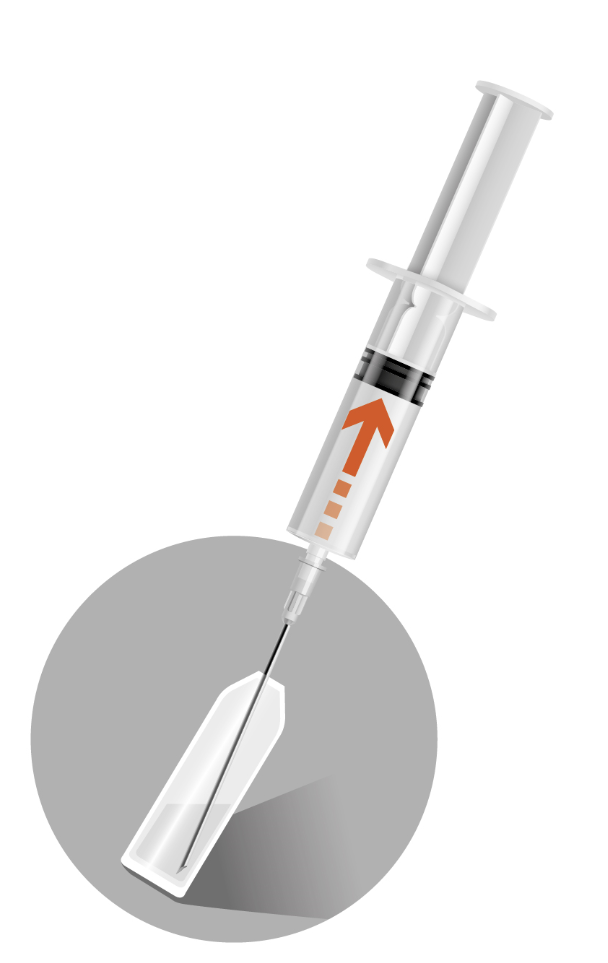
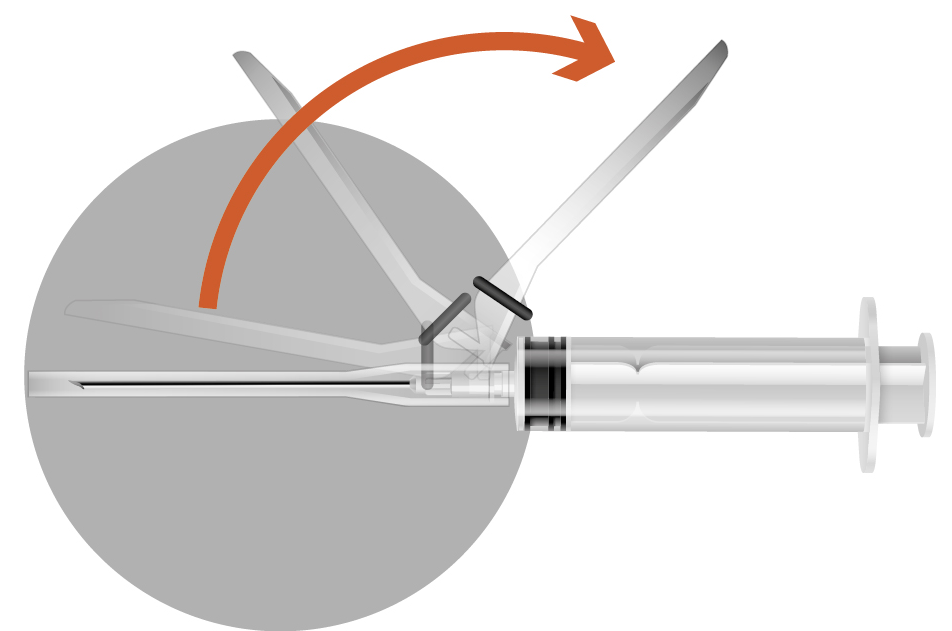
2г - Коли суспензія стане однорідною, опустити голку та набрати у шприц всю суспензію (не перевертаючи флакон). Незначну кількість суспензії, яка залишиться у флаконі, слід утилізувати. Ця кількість враховується у заявленому дозуванні. - Взятися за кольоровий роз’єм для приєднання голки. Зняти шприц з голки 1, що використовувалася для розведення. Нагвинтити на шприц голку 2. - Відвести захисний кожух від голки в напрямку циліндра шприца. Захисний кожух залишиться у встановленій Вами позиції. - Зняти захисний ковпачок з голки. - Заповнити голку, щоб усунути повітря зі шприца, та негайно виконати ін’єкцію. |
| ||||||
3. ВНУТРІШНЬОМ’ЯЗОВА ІН’ЄКЦІЯ | |||||||
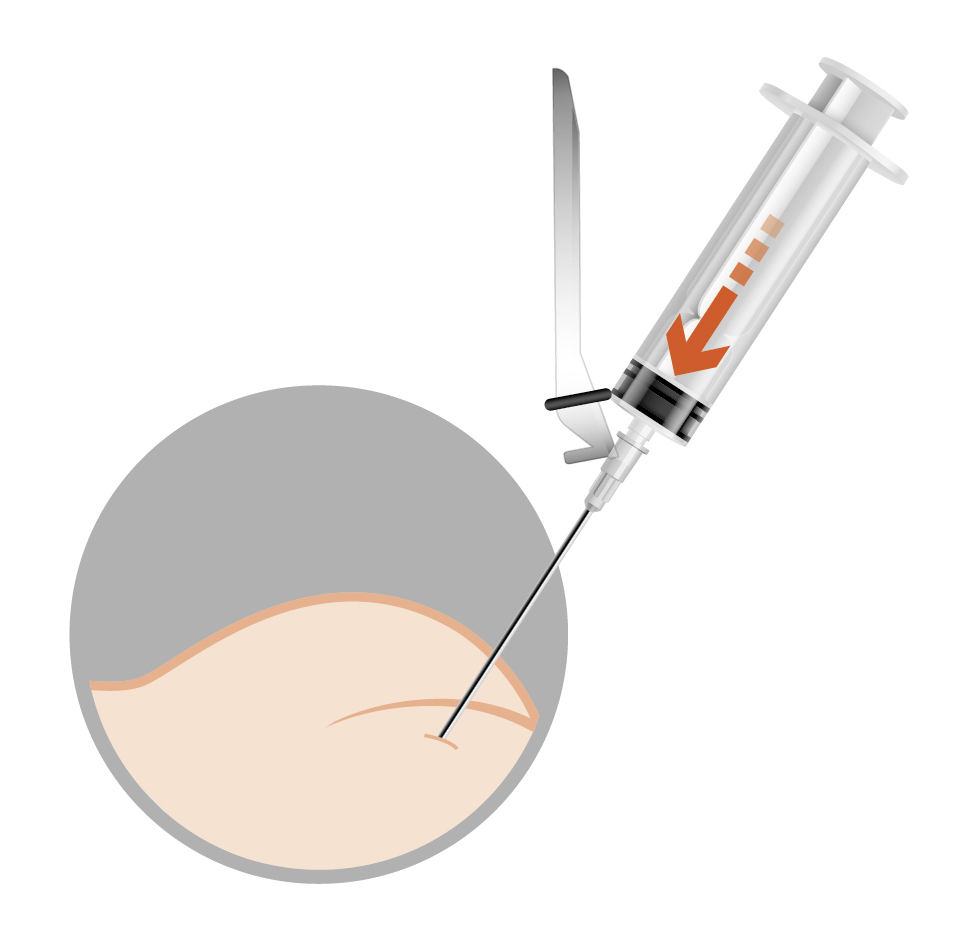
Для запобігання утворенню осаду слід негайно здійснити ін’єкцію в попередньо продезінфіковане місце. |
| ||||||
4. ПІСЛЯ ЗАСТОСУВАННЯ | |||||||
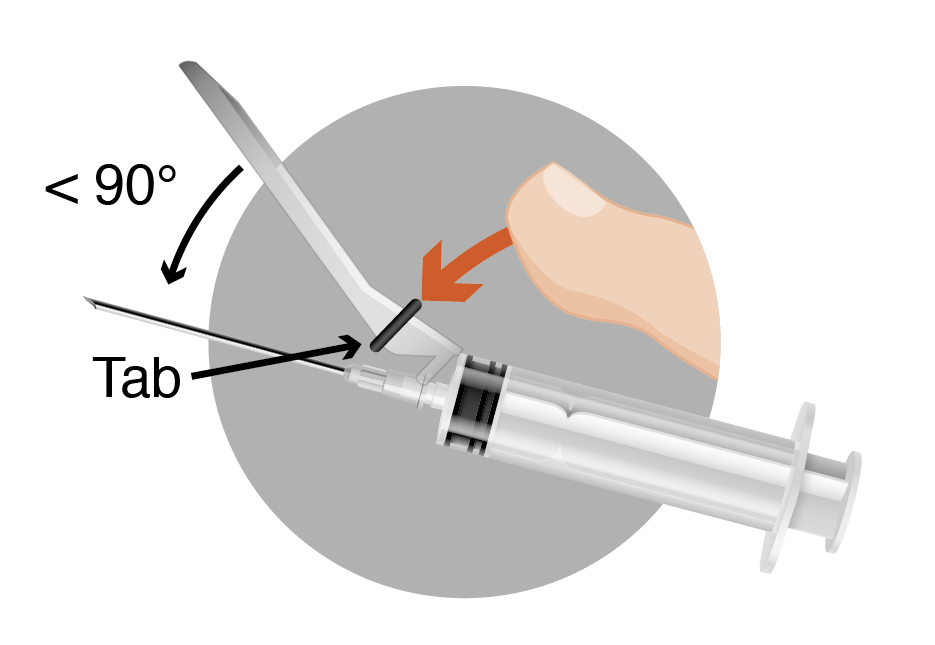
- Активуйте систему захисту одною рукою. - Примітка: завжди тримати палець за виступом. Два варіанти активації захисної системи - Метод А: натиснути на виступ пальцем або - Метод Б: притиснути кожух до плоскої поверхні - В обох випадках слід натискати міцним швидким рухом до виразно чутного клацання. - Візуально перевірити, що голка повністю заблокована. Використані голки, будь-які рештки невикористаної суспензії або інші відходи мають бути утилізовані відповідно до місцевих вимог. |
Метод А або
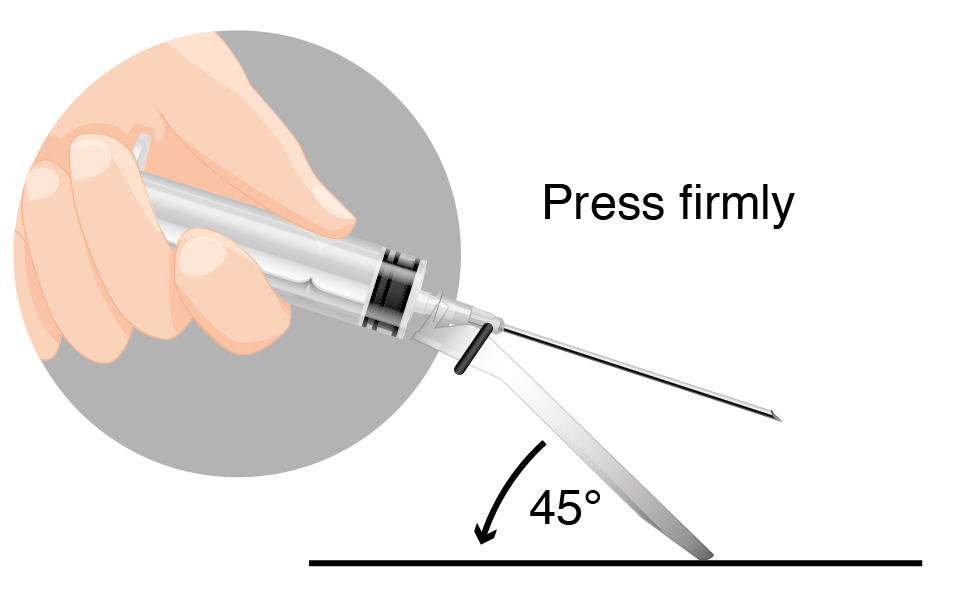 Метод Б Метод Б
| ||||||
Діти.
Диферелін® 3,75 мг призначений для лікування передчасного статевого дозрівання у дітей (початок захворювання у дівчаток віком до 8 років та у хлопчиків віком до 10 років) під ретельним наглядом дитячого ендокринолога, педіатра або ендокринолога з досвідом лікування передчасного статевого дозрівання центрального ґенезу.
Передозування.
У разі передозування рекомендовано симптоматичне лікування.
Побічні реакції.
Загальна переносимість у чоловіків (див. розділ «Особливості застосування»)
Через те, що пацієнти з місцевопоширеним чи метастатичним гормонзалежним раком передміхурової залози зазвичай є особами літнього віку та мають інші захворювання, поширені у пацієнтів цієї вікової групи, у більш ніж 90 % хворих, які брали участь у клінічних дослідженнях, спостерігалися небажані явища та часто було складно визначити причинно-наслідкові зв’язки.
За спостереженнями лікування іншими агоністами ГнРГ або хірургічної кастрації, найчастіші побічні реакції, пов’язані з терапією триптореліном, є наслідками його очікуваної фармакологічної дії. Вони включали припливи та зниження лібідо.
За винятком імуноалергічних реакцій (рідко) та реакцій в місці ін’єкції (< 5%), усі відомі побічні явища пов’язані зі змінами рівнів тестостерону.
Частота виникнення небажаних реакцій класифікується таким чином: дуже часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); рідко (≥1/10000, <1/1000). Частоту небажаних реакцій, що були зафіксовані у післяреєстраційний період, не можна визначити, тому вона зазначається як «невідома».
Зазначені нижче побічні реакції розцінювались як принаймні можливо пов’язані з терапією триптореліном. Виникнення більшості з них пов’язують з біохімічною або хірургічною кастрацією.
Клас / система органів | Дуже часто | Часто | Нечасто | Рідко | Частота невідома |
Інфекційні та паразитарні захворювання | Назофарингіт | ||||
Порушення з боку крові та лімфатичної системи | Анемія | Тромбоцитоз | |||
Порушення з боку імунної системи | Гіперчутливість | Анафілактична реакція | Анафілактичний шок | ||
Порушення з боку обміну речовин і розладів харчування | Анорексія, цукровий діабет, подагра, гіперліпідемія, підвищений апетит | ||||
Порушення з боку психіки | Зниження лібідо | Депресія, втрата лібідо, зміни настрою* | Безсоння, дратівливість | Сплутаність свідомості, зниження активності, стан ейфорії | Тривожність |
Порушення з боку нервової системи | Парестезія нижніх кінцівок | Запаморочення, головний біль | Парестезія | Порушення пам’яті | |
Порушення з боку органів зору | Погіршення зору | Порушення чутливості очей, порушення зору | |||
Порушення з боку органів слуху та рівноваги | Шум у вухах, вертиго | ||||
Порушення з боку серця | Відчуття серцебиття | Подовження інтервалу QT (див. розділи «Особливості застосування» та «Взаємодія з іншими лікарськими засобами та інші види взаємодій») | |||
Порушення з боку судин | Гарячі припливи | Артеріальна гіпертензія | Артеріальна гіпотензія | ||
Порушення з боку дихальної системи, органів грудної клітки та середостіння | Диспное, носова кровотеча | Ортопное | |||
Порушення з боку шлунково-кишкового тракту | Сухість у роті, нудота | Біль у животі, запор, діарея, блювання | Здуття живота, дисгевзія, метеоризм | ||
Порушення з боку шкіри та підшкірних тканин | Гіпергідроз | Акне, алопеція, еритема, свербіж, висипи, кропив’янка | Пухирі, пурпура | Ангіоневротичний набряк | |
Порушення з боку скелетно-м’язової та сполучної тканини | Біль у спині | Скелетно-м’язовий біль, біль у кінцівках | Артралгія, біль в кістках, м’язові судоми, м’язова слабкість, міалгія | Скутість у суглобах, набряк суглобів, кістково-м’язова скутість, остеоартрит | |
Порушення з боку нирок і сечовивідних шляхів | Ніктурія, затримка сечовипускан-ня | Нетримання сечі | |||
З боку репродуктивних органів і молочних залоз | Еректильна дисфункція (включаючи розлад еякуляції, порушення еякуляції) | Тазовий біль | Гінекомастія, біль у грудях, атрофія яєчок, біль у яєчках | ||
Загальні розлади і порушення у місці введення | Астенія | Реакції в місці ін’єкції (включаючи еритему, запалення та біль), набряк | Млявість, периферичний набряк, біль, озноб, сонливість | Біль у грудях, дистазія, грипоподібне захворювання, лихоманка | Відчуття нездужання |
Лабораторні та інструментальні дані | Збільшення маси тіла | Підвищення аланін амінотрансферази, підвищення аспартатамінотрансферази, підвищення рівня креатиніну в крові, підвищення артеріального тиску, підвищення рівня сечовини в крові, підвищення рівня гаммаглутамілтрансферази, зниження маси тіла | Підвищення активності лужної фосфатази в крові |
* Ця частота ґрунтується на спільній для всіх агоністів ГнРГ частоті побічних реакцій.
Трипторелін спричиняє тимчасове підвищення рівня тестостерону, що циркулює в крові, протягом першого тижня після введення першої ін’єкції лікарського засобу у пролонгованій формі. Під час початкового підвищення рівня тестостерону, що циркулює в крові, у деяких пацієнтів (≤ 5%) можливе погіршення симптомів наявного раку передміхурової залози («спалах»), що, як правило, виражається в симптомах з боку сечових шляхів (< 2%) та болях при метастатичному ураженні (5 %), які лікуються симптоматично. Симптоми мають тимчасовий характер і зазвичай зникають через 1-2 тижні.
Були зафіксовані поодинокі випадки загострення симптомів захворювання, обструкції уретри або спінальної компресії внаслідок метастазу. Тому пацієнти з метастатичним ураженням хребта та/або обструкцією верхніх або нижніх сечових шляхів мають перебувати під пильним наглядом протягом перших декількох тижнів терапії (див. розділ «Особливості застосування»).
Застосування агоністів ГнРГ при лікуванні раку передміхурової залози підвищує ризик втрати кісткової маси та може призвести до остеопорозу, а також підвищує ризик перелому кісток.
Було зафіксовано підвищення рівня лімфоцитів у пацієнтів, які проходили лікування аналогами ГнРГ. Такий вторинний лімфоцитоз, очевидно, пов’язаний з кастрацією, що була спричинена ГнРГ, та свідчить про участь гонадальних гормонів в інволюції тимуса.
У пацієнтів, які отримують тривалу терапію аналогом ГнРГ разом з опроміненням, може спостерігатися більша кількість побічних ефектів, особливо з боку шлунково-кишкового тракту, які пов’язані з застосуванням радіотерапії.
Загальна переносимість у жінок (див. розділ «Особливості застосування»)
Як наслідок зниження рівня естрогенів найбільш поширеними побічними ефектами (які очікуються у понад 10 % жінок) були головний біль, зниження лібідо, порушення сну, зміни настрою, диспареунія, дисменорея, генітальна кровотеча, синдром гіперстимуляції яєчників, гіпертрофія яєчників, тазовий біль, біль у животі, вульвовагінальна сухість, гіпергідроз, припливи й астенія.
Частота виникнення небажаних реакцій класифікується таким чином: дуже часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); рідко (≥1/10000, <1/1000). Частоту небажаних реакцій, що були зафіксовані у післяреєстраційний період, не можна визначити, тому вона зазначається як «невідома».
Зазначені нижче побічні реакції розцінювались як принаймні можливо пов’язані з терапією триптореліном. Виникнення більшості з них пов’язують з біохімічною або хірургічною кастрацією.
Клас / система органів | Дуже часто | Часто | Нечасто | Частота невідома |
Порушення з боку імунної системи | Гіперчутливість | Анафілактичний шок | ||
Порушення з боку обміну речовин і розладів харчування | Зниження апетиту, затримка рідини | |||
Порушення з боку психіки | Розлади сну (включаючи безсоння), зміни настрою, зниження лібідо | Депресія*, знервованість | Афективна лабільність, тривожність, депресія**, дезорієнтація | Сплутаність свідомості |
Порушення з боку нервової системи | Головний біль | Запаморочення | Дисгевзія, гіпестезія, непритомність, розлади пам’яті, порушення уваги, парестезія, тремор | |
Порушення з боку органів зору | Сухість очей, погіршення зору | Порушення зору | ||
Порушення з боку органів слуху та рівноваги | Вертиго | |||
Порушення з боку серця | Відчуття серцебиття | |||
Порушення з боку судин | Гарячі припливи | Артеріальна гіпертензія | ||
Порушення з боку дихальної системи, органів грудної клітки та середостіння | Диспное, носова кровотеча | |||
Порушення з боку шлунково-кишкового тракту | Нудота, біль у животі, дискомфорт у животі | Здуття живота, діарея, сухість у роті, метеоризм, виразковий стоматит, блювання | ||
Порушення з боку шкіри та підшкірних тканин | Акне, гіпергідроз, себорея | Алопеція, сухість шкіри, гірсутизм, оніхолізис, свербіж, висип | Ангіоневротичний набряк, кропив’янка | |
Порушення з боку скелетно-м’язової та сполучної тканини | Артралгія, м’язові спазми, біль у кінцівках | Біль у спині, міалгія | М’язова слабкість | |
З боку репродуктивних органів і молочних залоз | Патології молочних залоз, диспареунія, генітальна кровотеча (включаючи вагінальну кровотечу, кровотечу відміни), синдром гіперстимуляції яєчників, гіпертрофія яєчників, тазовий біль, вульвовагінальна сухість | Біль у грудях | Кровотеча при статевому акті, цистоцеле, порушення менструального циклу (включаючи дисменорею, метрорагію та менорагію), кіста яєчника, виділення з піхви | Аменорея |
Загальні розлади і порушення у місці введення | Астенія | Реакції в місці ін’єкції (включаючи біль, набряк, еритему та запалення), периферичний набряк | Лихоманка, відчуття нездужання | |
Лабораторні та інструментальні дані | Збільшення маси тіла | Зменшення маси тіла | Підвищення рівня лужної фосфатази в крові, підвищення артеріального тиску |
*Довготривале застосування:ця частота ґрунтується на спільній для всіх агоністів ГнРГ частоті побічних реакцій.
**Короткотривале застосування:ця частота ґрунтується на спільній для всіх агоністів ГнРГ частоті побічних реакцій.
На початку лікування, під час тимчасового підвищення рівня естрадіолу в крові, дуже часто (≥ 10%) можуть загострюватися симптоми, характерні для ендометріозу, зокрема тазовий біль, дисменорея. Такі симптоми мають тимчасовий характер і зазвичай минають через 1-2 тижні.
Протягом одного місяця після проведення першої ін’єкції можливе виникнення генітальної кровотечі, включаючи метрорагію та менорагію.
При лікуванні безпліддя з використанням гонадотропних гормонів можливе виникнення синдрому гіперстимуляції яєчників. Можуть спостерігатися гіпертрофія яєчників, диспное, тазові болі та/або болі в животі.
Тривале застосування аналогів ГнРГ може призвести до втрати кісткової маси та є фактором ризику розвитку остеопорозу.
Рак молочної залози
Найчастішими побічними реакціями на тлі терапії триптореліном у період до 5 років у поєднанні або з тамоксифеном, або з інгібітором ароматази у дослідженнях TEXT і SOFT були припливи, порушення з боку скелетно-м’язової системи, втомлюваність, безсоння, гіпергідроз, вульвовагінальна сухість та депресія.
Небажані реакції, про які повідомляли на тлі застосування триптореліну в поєднанні з тамоксифеном (N=2325) або в поєднанні з екземестаном (N=2318), представлено у наступній таблиці та класифіковано за частотою: дуже часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); рідко (≥1/10000, <1/1000).
Клас / система органів | Дуже часто | Часто | Нечасто | Рідко |
Порушення з боку імунної системи | Гіперчутливість | |||
Порушення з боку ендокринної системи | Цукровий діабет (непереносимість глюкози), гіперглікемія | |||
Порушення з боку психіки | Безсоння, зниження лібідо, депресія | |||
Порушення з боку нервової системи | Церебральна ішемія, крововилив у центральну нервову систему | |||
Порушення з боку серця | Ішемія міокарду | Подовження інтервалу QT | ||
Порушення з боку судин | Гарячі припливи, артеріальна гіпертензія | Емболія | ||
Порушення з боку шлунково-кишкового тракту | Нудота | |||
Порушення з боку шкіри та підшкірних тканин | Гіпергідроз | |||
Порушення з боку скелетно-м’язової та сполучної тканини | Порушення з боку скелетно-м’язової системи, остеопороз | Перелом | ||
Порушення з боку нирок і сечовивідної системи | Нетримання сечі | |||
З боку репродуктивних органів і молочних залоз | Диспареунія, вульвовагінальна сухість | |||
Загальні розлади і порушення у місці введення | Втомлюваність | Реакції в місці ін’єкції |
Зазначені вище побічні реакції слід мати на увазі додатково до інформації про побічні реакції триптореліну у чоловіків і жінок у попередніх таблицях для повного опису профілю побічних реакцій при застосуванні супресора функції яєчників у комбінації або з екземестаном, або з тамоксифеном.
Остеопороз спостерігали з більш високою частотою на тлі застосування триптореліну з екземестаном, аніж з тамоксифеном (39% порівняно з 25%) (див. розділ «Особливості застосування»).
Порушення з боку скелетно-м’язової системи та переломи також частіше відмічали у пацієнток, які отримували трипторелін у поєднанні з екземестаном, аніж з тамоксифеном (відповідно 89% порівняно з 76% та 6,8% порівняно з 5,2%).
При застосуванні триптореліну у комбінації або з екземестаном, або з тамоксифеном повідомляли про артеріальну гіпертензію як про передбачуване побічне явище, що виникало дуже часто (відповідно 23% та 22%).
На тлі застосування триптореліну у поєднанні або з екземестаном, або з тамоксифеном виникали часто випадки гіперглікемії та цукрового діабету як передбачуване побічне явище (гіперглікемія - відповідно 2,6% та 3,4%; цукровий діабет - 2,3% та 2,3%).
Загальна переносимість у дітей (див. розділ «Особливості застосування»)
За спостереженнями лікування іншими агоністами ГнРГ, найчастіші побічні реакції, пов’язані з терапією триптореліном під час клінічних досліджень, виникали через його очікувану фармакологічну дію: серед цих ефектів була вагінальна кровотеча, іноді низької інтенсивності (кровомазання).
Частота виникнення небажаних реакцій класифікується таким чином: дуже часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); рідко (≥1/10000, <1/1000). Частоту небажаних реакцій, що були зафіксовані у післяреєстраційний період, не можна визначити, тому вона зазначається як «невідома».
Зазначені нижче побічні реакції вважалися принаймні можливим наслідком лікування триптореліном.
Клас / система органів | Дуже часто | Часто | Нечасто | Частота невідома |
Порушення з боку імунної системи | Гіперчутливість | Анафілактичний шок (спостерігали у дорослих чоловіків і жінок) | ||
Порушення з боку обміну речовин і розладів харчування | Ожиріння | |||
Порушення з боку психіки | Мінливий настрій | Афективна лабільність, депресія, знервованість | ||
Порушення з боку нервової системи | Головний біль | |||
Порушення з боку органів зору | Погіршення зору | Порушення зору | ||
Порушення з боку судин | Гарячі припливи | Артеріальна гіпертензія | ||
Порушення з боку дихальної системи, органів грудної клітки та середостіння | Носова кровотеча | |||
Порушення з боку шлунково-кишкового тракту | Біль у животі | Блювання, запор, нудота | ||
Порушення з боку шкіри і підшкірних тканин | Акне | Свербіж, висип, кропив'янка | Ангіоневротичний набряк | |
Порушення з боку скелетно-м’язової і сполучної тканини | Біль у шиї | Міалгія | ||
Порушення з боку репродуктивних органів і молочних залоз | Вагінальна кровотеча (у т. ч. вагінальний крововилив), кровотеча відміни, крововилив у матці, вагінальні виділення, кровомазання | Біль у грудях | ||
Загальні розлади і порушення у місці введення | Реакції у місці ін’єкції (у т. ч. біль у місці ін’єкції, подразнення місця ін’єкції та запалення в місці ін’єкції) | Нездужання | ||
Лабораторні та інструментальні дані | Підвищена маса тіла | Підвищений рівень пролактину в крові, підвищений артеріальний тиск |
Повідомлення про побічні реакції
Повідомлення про побічні реакції після реєстрації лікарського засобу є важливими. Це забезпечує постійний моніторинг співвідношення користь/ризик застосування лікарського засобу. Медичних працівників просять повідомляти про будь-які підозрювані побічні реакції через національну систему повідомлень.
Термін придатності.3 роки.
Умови зберігання.
Зберігати в оригінальній упаковці при температурі не вище 25 °С.
Зберігати у недоступному для дітей місці.
Несумісність.
Змішування порошку з розчинником слід виконувати безпосередньо перед ін’єкцією. Слід використовувати тільки той розчинник, що міститься в упаковці.
Упаковка.1 флакон з порошком у комплекті з розчинником по 2 мл (маніт (Е 421), вода для ін’єкцій) в ампулі, шприцом для одноразового використання та двома голками (у блістерній упаковці) в картонній коробці.
Категорія відпуску.За рецептом.
Виробник.
ІПСЕН ФАРМА БІОТЕК.
Місцезнаходження виробника та адреса місця провадження його діяльності.
Парк д’aктівіте дю Плато де Сінь департаментська дорога № 402, 83870 СІНЬ, Франція/
Заявник.
ІПСЕН ФАРМА.
Місцезнаходження заявника.
65, набережна Жорж Горс-92100 Булонь Бійанкур, Франція.

На сайті наведено виключно офіційні оновлені інструкції без перекладів та скорочень.
Інформація про лікарські засоби представлена на сайті для ознайомлення, не є приводом для самолікування та не є рекламою лікарських засобів.
 Важливо! До кожного лікарського засобу, який ви купуєте, обов’язково має додаватися інструкція про застосування лікарського засобу.
Важливо! До кожного лікарського засобу, який ви купуєте, обов’язково має додаватися інструкція про застосування лікарського засобу.
Тримайте всі інструкції до препаратів Домашньої аптечки під рукою – завантажуйте мобільний додаток Ліки Контроль БЕЗКОШТОВНО